De 12 éléments connus avant 1700, on est passé à plus de 80 éléments connus en 1900. L'enjeu était à cette époque de pouvoir enseigner et transmettre ce savoir chimique. En effet, jusque-là, l'enseignement de la chimie et de ses éléments se présentait sous la forme de longues listes avec leurs propriétés totalement décorrélées les unes des autres.
Présentation
Comme le montre le tableau suivant (voir fig. 1), les chimistes du XIXè siècle ont constaté l'explosion démographique des éléments. De 12 éléments connus avant 1700, on est passé à plus de 80 élements connus en 1900. L'enjeu était à cette époque de pouvoir enseigner et transmettre ce savoir chimique. En effet, jusque-là, l'enseignement de la chimie et de ses éléments se présentait sous la forme de longues listes avec leurs propriétés totalement décorrélées les unes des autres.
| Avant 1700 | 1700 - 1799 | 1800 - 1849 | 1850 - 1899 |
|
Antimoine Argent Arsenic Carbone Cuivre Etain Fer Mercure Or Phosphore Plomb Soufre
(12) |
Azote Béryllium Bismuth Chlore Chrome Coballt Fluor Hydrogène Manganèse Molybdène Nickel Oxygèène Platine Strontium Tellure Titane Tungstène Uranium Yttrium Zinc Zirconium
(21) |
Aluminium Baryum Bore Brome Cadmium Calcium Cérium Erbium Iode Lanthane Iridium Lithium Magnésium Nobium Osmium Palladium Potassium Rubidium Sélénium Silicium Sodium Tantale Thorium Vanadium (24) |
Actinium Argon Césium Dysprosium Gadolinium Gallium Germanium Hélium Holmium Indium Krypton Néodyme Néon Polonium Praséodyme Radium Rhodium Ruthénium Samarium Scandium Thallium Thulium Xénon Ytterbium (24) |
De longues recherches se sont déroulées pendant près d'un siècle pour obtenir le tableau connu aujourd'hui. En 1869, Dmitri Ivanovitch Mendeleïev classe l’ensemble des éléments en un système périodique suivant l’ordre de progression des poids atomiques. Son nom aujourd’hui figure dans tous les livres de chimie.
Mendeleïev figure souvent comme un devin, un prophète qui, dans une intuition fulgurante, un éclair de génie, aurait anticipé non seulement sur l’expérience, en prédisant des éléments inconnus, mais aussi sur les théories quantiques du XXème siècle. Mais cela ne serait-il pas simplement dû au génie et à la méthode de ce chimiste russe ? En effet certains chercheurs, notamment Oliver Sacks dans le New York Times qualifie la découverte de Mendeleïev comme la « meilleure idée, histoire et invention de ce dernier millénaire ».
Néanmoins, cette interprétation du passé à partir de la science contemporaine est surnommée « whig history » par les historiens anglais. « L’histoire postiche » est très répandue dans les cours et congrès scientifiques. Cherchant dans le passé les jalons qui mènent aux théories d’aujourd’hui, les scientifiques ont tendance à schématiser l’histoire. Eliminant les fausses pistes et les impasses, ils inventent une voie royale conduisant à la science présente.
Nous allons au cours de ce plan détaillé tâcher de présenter la démarche scientifique qui a conduit à l'élaboration de ce tableau ; démarche qui a débuté bien avant Mendeleïev.
Les travaux réalisés avant Mendeleïev
Les premières règles du langage chimique avec Guyton
Les règles de Guyton sont détaillés dans son ouvrage paru en 1782 : « Mémoire sur les dénominations chimiques, la nécessité d’en perfectionner le système, et les règles pour y parvenir ».
Les principales règles sont :
- Chaque substance : un nom et pas une circonlocution.
- Le nom évoque les constituants et pas celui qui a découvert.
- Si composition incertaine : dénomination ne signifiant rien.
- Nouveaux termes à partir du latin et du grec.
(exemples : « sel marin à base de terre pesante » : muriate de barote ; « sel de succin retiré par la cristallisation » : acide succinique cristallisé ; « sucre de Saturne » : acétate de plomb ; « lune cornée » : muriate d’argent)
La classification de Lavoisier
En 1789, dans son ouvrage « Traité élémentaire de chimie présenté dans un ordre nouveau et d’après les découvertes modernes », Lavoisier expose les principes de sa classification des éléments chimiques :
5 classes
- 5 éléments qui s’approchent le plus de l’état de simplicité : lumière, calorique, oxygène, hydrogène, azote.
- 25 bases acidifiables.
- 17 substances métalliques.
- 5 terres.
- 3 alkalis.
Il s'agit de la première organisation sous forme de tableau ; elle clarifie certaines différences mais ne révèle pas la périodicité des propriétés des éléments classés (exemple : les métaux sont classés par ordre alphabétique en français).
Notion de poids atomique
- Introduite par Dalton en 1808.
- But : Comparer les masses des différents atomes ; unité : H (plus petite masse).
- Système de Dalton confirmé par lois sur les gaz de Gay-Lussac : « Les volumes de deux gaz qui se combinent sont entre eux dans des rapports simples »
- Loi d’Avogadro-Ampère fait la jonction : « Des volumes égaux de gaz, pris à la même température et à la même pression, contiennent le même nombre de molécules » → détermine le poids atomique d’après la densité gazeuse.
- 1860 Karlsruhe : système cohérent de poids atomiques qui comportait cependant certaines erreurs : Mendeleïev n'hésitera pas à « corriger » certaines valeurs pour réaliser sa classification.
Les triades de Johann Döbereiner
- Basé sur relation entre poids atomiques (demi-somme des poids équivalents) et propriétés chimiques.
- Eléments groupés par trois.
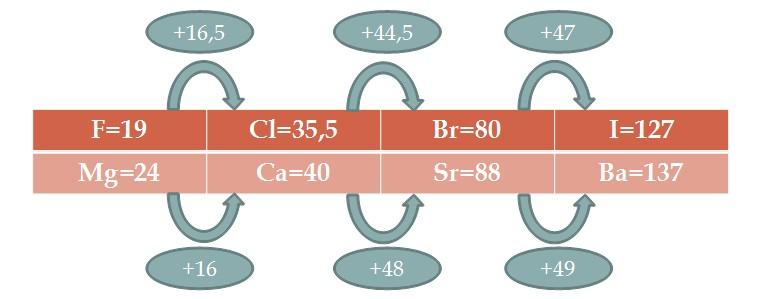
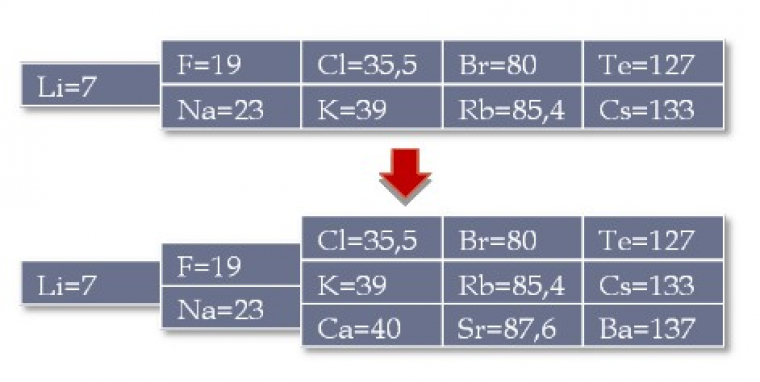
- 1817 : 1ère triade Sr, Ca, Ba → alcalino-terreux Sr(88) = [Ca(40) + Ba(137)] / 2
- 1829 : deux autres « triades ».
- halogènes : même facilité à former ion monoatomique négatif Br(80) = [Cl(35,5) + I(127)] / 2
- métaux alcalins : Na(23) = [Li(7) + K(39)] / 2
- 1850 : environ 20 triades.
Les tétrades de Jean-Baptiste Dumas
- 1859 : Ajout d’un quatrième élément à la triade.
- Progressions similaires d’une tétrade à l’autre.
- Applicable à un plus grand nombre d’éléments.
- L’incrément constaté par Dumas mesure précisément la longueur de la période qui sépare ces deux éléments.
Mise en évidence de la périodicité
La vis tellurique de Chancourtois (1862)
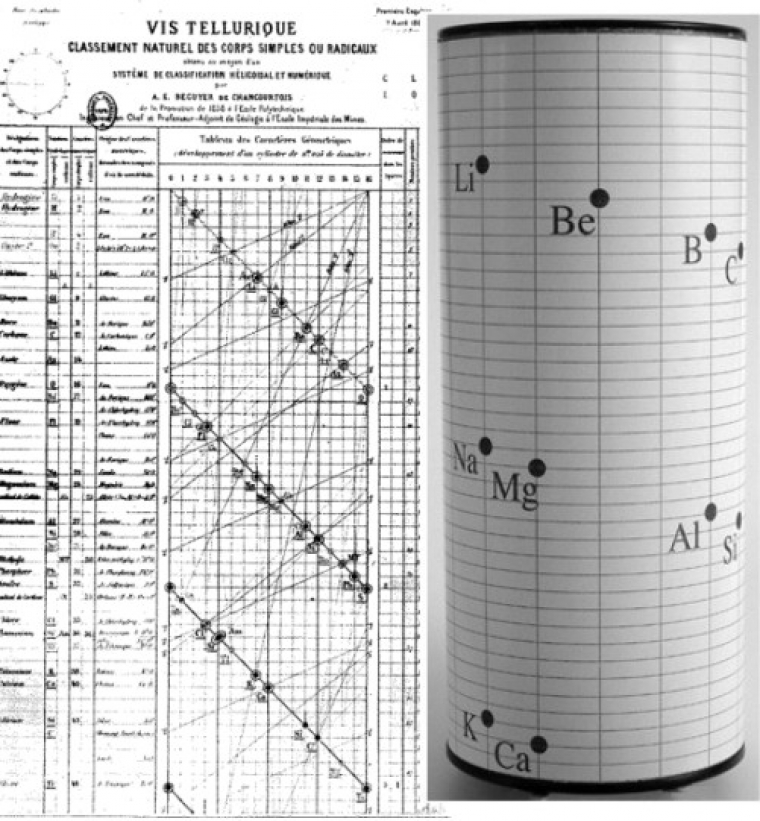
Il est le premier à remarquer la périodicité des propriétés chimiques.
-
Classement des éléments chimiques en fonction de leur masse atomique croissante.
-
Cylindre divisé en seize parties, les éléments aux propriétés similaires apparaissent l'un au-dessus de l'autre.
-
Il retrouve certaines triades et tétrades alignées (ex: O:16, S:32, Se:79, Te:128).
-
Son classement ne retient pas l'attention de la communauté scientifique mais il est d'une grande avancée d'un point de vue conceptuel.
De la chimie empirique à la chimie raisonnée
Alors que la plupart des chercheurs de l’époque ne s’intéressent qu’aux relations arithmétiques et peu aux analogies de propriétés chimiques entre éléments, trois scientifiques vont aller à contre courant.
Plutôt que de privilégier des relations de parentés locales, Newlands, Odling & Mendeleïev recherchent une loi générale basée sur l'utilisation des poids atomiques et permettant la prévision des éléments encore inconnus.
Loi des octaves de John Newlands (1863)
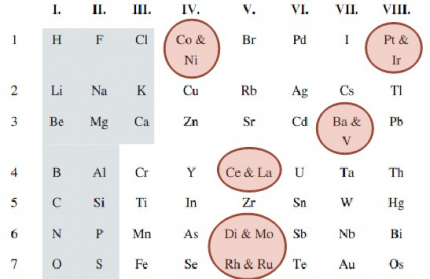
J. Newlands propose une organisation par masse atomique croissante en regroupant sur une ligne les éléments ayant des propriétés chimiques similaires. On peut d'ailleurs trouver deux éléments dans une même case.
Avancées
-
Périodicité globale jusqu'au calcium;
-
Inversion de Te et I;
-
Il est le premier à prévoir l'existence d'éléments non encore découverts;
-
Identification d’une nouvelle triade Si-Sn avec élément médian à découvrir (Ge).
Faiblesses
-
Absence de case vide.
-
Problème de périodicité.
-
Poids atomiques incorrects.
-
Que 51 éléments (sur 60).
-
Mal accueilli par ses pairs.
Notion d’éléments manquants par William Odling (~1860)
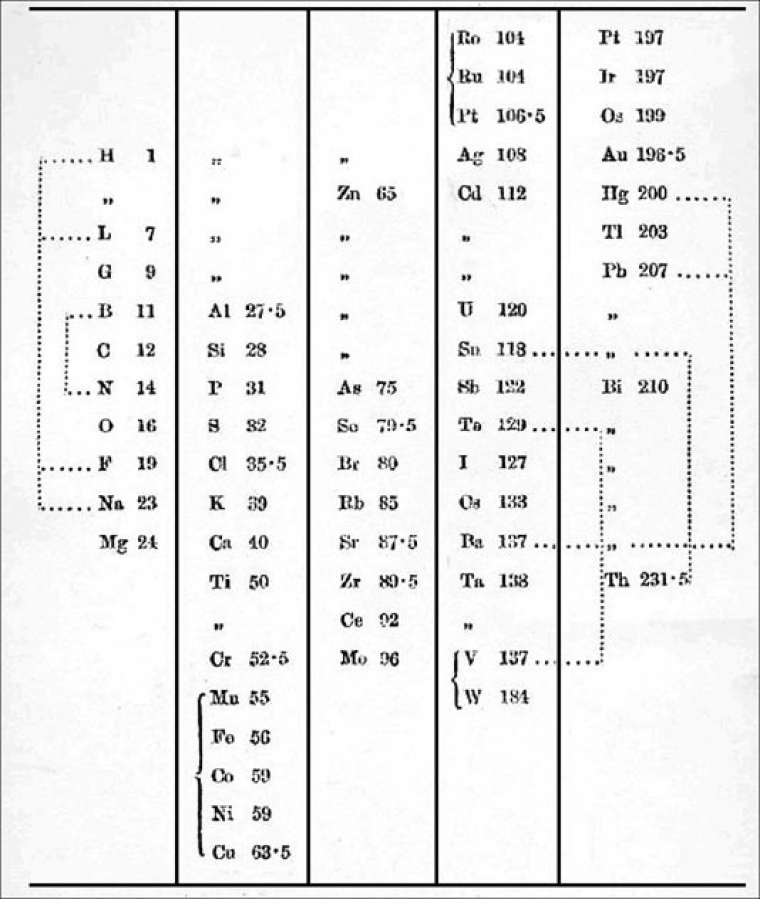
Il propose une classification proche de celle publiée par Mendeleïev.
Avancées
-
1er à introduire des places vacantes.
-
Pt, Hg, Th et Pb dans les bons groupes.
-
57 éléments sur 60 connus à l'époque.
-
Fidèle à l’ordre de croissance des poids atomiques.
Faiblesses
-
Régression dans les publications suivantes.
-
Action négative à l'encontre de Newlands.
Introduction de la valence par Lothar Meyer (1870)
-
1864 : Première édition du tableau à 28 éléments, classés en 6 familles : vers la forme moderne.
-
1868 : Second tableau : véritable classification périodique (comprenant même les métaux de transition).
Avancées
-
Périodes de longueurs variables.
-
Il réorganise tout l’exposé de la chimie minérale à partir de sa classification.
Faiblesses
-
Pas de correction de poids atomiques.
-
N’anticipe pas les propriétés des éléments manquants.
Comment Mendeleïev s’est-il démarqué de ses prédécesseurs ?
La quête d’une loi
Comme Newlands et Odling, Mendeleïev privilégie la recherche d’une loi générale à la recherche d’une classification. Une loi générale permet les prévisions d’éléments inconnus, les corrections de poids atomiques, les inversions…
La loi périodique (1869) : « Les propriétés des corps simples et composés dépendent d’une fonction périodique des poids atomiques des éléments, pour la seule raison que ces propriétés sont elles-mêmes les propriétés des éléments dont ces corps dérivent ».
Il a une confiance absolue en sa découverte et la considère comme plus importante que le tableau lui-même.
Corps simples ou éléments?
Depuis Lavoisier, corps simple et élément sont synonymes. Mais Mendeleïev apporte la distinction et classe par éléments !
Lavoisier explique les propriétés des corps composés par celles des corps simples ; Mendeleïev explique les propriétés des corps simples par celles des éléments.
Les chemins de la découverte
Mendeleïev raconte ses démarches dans Principes de la chimie rédigé entre 1868 et 1871.
D’après lui, le secret de sa réussite a été la décision de comparer les halogènes et les métaux alcalins :
Il écrira ainsi : « Vers 1860, le terrain était déjà tout préparé pour cette loi, et si elle n’a été énoncée que plus tard, la cause réside, à mon avis, en ce que l’on comparait entre eux les éléments semblables, en laissant de côté les éléments dissemblables ».
On est donc bien loin d'une intuition unique mais au contraire d'un long chemin de réflexion de différents scientifiques.
La légende retient une découverte en un seul jour de réflexion, le 17 février 1869. Mais en réalité, Mendeleïev a beaucoup tâtonné. Il hésite d’abord entre tableau et spirale pour retenir la forme actuelle qui lui permet de mieux souligner la périodicité.
On constate que dès la publication de ce tableau, Mendeleïev prévoit la place pour des éléments encore inconnus à l'époque. Il leur donnera le préfixe « Eka- » de l'élément auquel ils se rattachent en termes de propriétés chimiques. Ainsi l'Eka-Silicium correspond au Germanium, découvert une quinzaine d'années plus tard.
| Prédictions | Déterminations |
|
Eka-alumium Poids atomique : 68 Volume atomique : 11,5 ... |
Gallium (1875) 69,9 11,7
|
|
Eka-Bore Poids atomique : 44 Oxyde : Eb2O3 Sulfate : Eb2(SO4)3 ... |
Scandium (1879) 43,79 Sc2O3 Sc2(S04)3
|
|
Eka-Silicium Poids atomique : 72 Volume atomique : 13 Oxyde : EsO2 Chlorure : EsCl4 Teb du chlorure : <100°C Densité du chlorure : 1,9 ... |
Germanium (1886) 72 13,2 GeO2 GeCl4 86°C 1,887
|
Les améliorations ultérieures
A la fin du XIXème siècle, un souci surgit lors de la découverte des gaz rares. La découverte de l’argon par William Ramsay et Lord Rayleigh (1894), du néon par Ramsay et Morris Travers (1898) pose problème : il n'y a pas de places prévues par Mendeleïev dans son tableau pour cette nouvelle famille.
Il n'est d'ailleurs pas étonnant que Mendeleïev n'ait pas prévu cette famille des gaz rares. Elle est en effet composée d'éléments à couche électronique saturée et donc inertes ; difficile à mettre en évidence à l'époque !
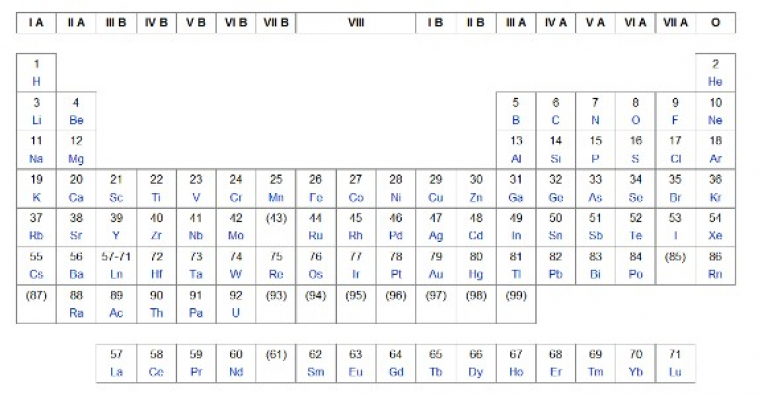
La solution est alors un classement en numéro atomique Z plutôt qu’en masse atomique (théoricien hollandais Anton Von den BROEK, 1913). Ce classement est rendu possible grâce à Henry Moseley qui établit une relation entre Z et le spectre de rayons X.
Le concept concernant l'ajout des actinides sera réalisé par Glenn Seaborg en 1944.
Conclusion
Mendeleïev n’était pas un marginal de son époque, beaucoup de chercheurs de divers horizons se sont penchés sur ce problème de classification.
De Lavoisier à Glenn Searborg, il y a près de deux siècles de recherches et d'échanges scientifiques pour parvenir au tableau que nous connaissons aujourd'hui !
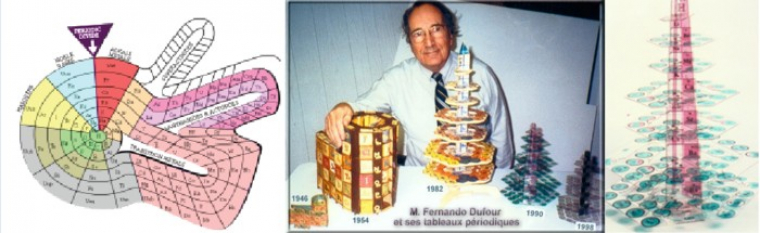
De nos jours, il existe encore quelques recherches afin d’améliorer ce tableau. Citons le tableau « escargot » de Theodor Benfey en 1960 afin de rémédier aux discontinuités du tableau standard ou encore de nombreux tableaux 3D de Fermando Dufour.
Bibliographie
- Éléments d’histoire des sciences, Serres, Chap 19, Bernadette Bensaude-Vincent
- Tableaux et langages de la chimie, Essai sur la représentation, François Dagognet
- La classification périodique des éléments, la meilleure invention du millénaire, Dr. Jean-Claude Roy
- Eléments et atomes, Petite histoire d'un modèle d'après ses textes fondateurs, Thérèse Mayer