Les rois et reines de l’Égypte antique sont représentés avec des yeux fardés de noir comme l’attestent de nombreuses iconographies égyptiennes antiques. Outre le caractère esthétique, ce maquillage des yeux leur assurait un liquide lacrymal enrichi de façon constante en ions Pb2+ qui protégeait les yeux en permanence par une riche population de macrophages constituant une barrière antibactérienne redoutable.
Musée du Louvre
Introduction
Les rois et reines de l’Égypte antique (Aménophis, Ramsès, etc) sont représentés avec des yeux fardés de noir comme l’attestent de nombreuses iconographies égyptiennes antiques (figure 1). Ainsi, le khôl (ou kohol), fard noir, a longtemps été assimilé à un signe de distinction de la noblesse égyptienne. Cependant, des fresques et statuettes dont les premières datent d’il y a 4500 ans, ont permis de constater que ce maquillage était porté par la plupart des égyptiens y compris les enfants.
Histoire de la découverte d’une vertu thérapeutique
Les papyrus et les fresques retrouvés ont en effet montré qu’il s’agissait d’une tradition liée à la volonté de s’assurer la protection d’Horus en dessinant sur soi l’œil magique d’Oudjat. Cet œil magique était censé protéger celui qui le porte contre les puissances maléfiques comme par exemple, dans la vie après la mort.
De nombreux flacons et pots ont pu être retrouvés intacts dans les tombes égyptiennes. En fonction du statut social du défunt, bambou ou pots de belle facture étaient utilisés pour contenir le fard. L’étude de résidus de poudre retrouvés dans des pots à khôl, conservés au musée du Louvre a permis de déterminer la composition chimique de ces fards.
Dans ces compositions, on retrouve des dérivés de plomb : galène, laurionite, phosgénite et cérusite (figure 2). Ces derniers sont liés par une substance grasse afin d'obtenir une pâte permettant l'application sur le bord des paupières :
Les cristaux de galène ont été identifiés comme provenant de Gebel el‐Zeit à coté de la mer Rouge. L’origine des cristaux trouvés est déterminée par le pourcentage d’impuretés de ce dernier. La galène confère au fard sa qualité de « gloss » suite à un broyage minutieux, les cristaux possèdent alors un diamètre d’environ 1 μm. Ceci est dû aux facettes régulières des cristaux qui réfléchissent extraordinairement bien la lumière incidente, tout comme nos maquillages actuels.
Les grains de cérusite, de couleur blanche et d’aspect poreux, servaient a priori d’absorbant d’ancrage pour les molécules grasses constituant le support pâteux de l’onguent.
La laurionite (Pb(OH)Cl) présente dans ces compositions, est un composé présent en très faibles quantités dans la nature. Elle est issue d'un processus de synthèse afin d’en faire une production de masse. Le papyrus d’Ebers (1600 av. J.C.) explique pourquoi ce composé a été largement synthétisé. Ce traité médical, recueillant de nombreuses « recettes » destinées à reconnaître et à traiter une grande variété de maladies, indique que le khôl est destiné à traiter ou à prévenir des maladies des yeux. On attribue aujourd’hui cette propriété à la laurionite qui présente la bonne solubilité dans le liquide lacrymal.
La population égyptienne était concentrée autour du Nil et son delta. Cet environnement fortement humide et marécageux est propice au développement d'infections endémiques.
Synthèse de la laurionite
Le processus originel de synthèse de la laurionite a été retrouvé dans les travaux d'un médecin grec Dioscoride (Ier siècle ap. J.C). Il indique que la laurionite était « un très bon onguent pour la protection des yeux, pour les plaies infectées, la réduction des rides, et le soin de bien d'autres parties du corps ».
La recette est décrite en ces termes : « Après avoir mélangé une livre d’écume d’argent [PbO] à cinq drachmes de sel de roche [NaCl], verser dessus de l’eau tiède, et remuer très vigoureusement trois fois par jour [...] Laisser le mélange reposer, éliminer l’excès d’eau, puis ajouter du sel de roche et de l’eau tiède. Répéter l’ensemble de ces opérations trois fois par jour pendant 30 jours jusqu’à ce que la solution ait perdu toute sa causticité [basicité] ».
La recette peut se traduire, en termes chimiques, par l’équation suivante :
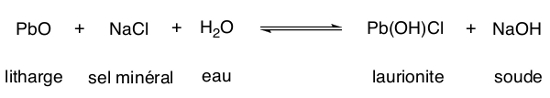
On forme ainsi un complexe du plomb en solution aqueuse. Les complexes des métaux de transition, dans ces conditions, ne sont stables que dans des gammes de pH déterminées. Il est possible grâce aux données thermodynamiques de prévoir la stabilité (donnée par les potentiels rédox) des complexes en fonction du pH et éventuellement de la concentration en ligand, comme ici, les ions chlorures. Ces diagrammes sont appelés diagrammes de Pourbaix.
En interprétant celui du plomb (figure 4), on se rend compte que la recette proposée par Dioscoride pose un problème majeur : la laurionite a un domaine de stabilité limité à un pH compris entre 5 et 8.
Or l'équation de la réaction montre que de la soude (NaOH) est formée en même temps que la laurionite. Le pH devient donc de plus en plus basique au cours de la réaction, ce qui devrait finalement favoriser la transformation de la Laurionite en Blixite.
Pour palier ce problème, le protocole propose d'éliminer le surnageant « caustique » trois fois par jour pendant un mois et d'ajouter à chaque fois de l'eau et du chlorure de sodium. Cela permet deux choses :
- réguler (de façon totalement empirique certes, mais tout de même précise) le pH et empêcher la formation de la blixite ;
- appliquer le principe de Le Chatelier : en éliminant un des produits de la réaction, l'équilibre se déplace vers la droite et à chaque cycle en ajoutant l'eau et le sel, ils ajoutent un des réactifs jusqu'à consommer totalement l'oxyde de plomb.
La phosgénite dérive de la laurionite. Elle est due à la présence de carbonate dans l’eau.
Ainsi les égyptiens avaient trouvé une méthode pour rendre totale et sélective une réaction qui ne peut l'être sans intervention. N'est-on pas ici devant un procédé chimique au sens moderne ? La première synthèse chimique inorganique connue ?
Vertus Médicinales
L'environnement fortement humide dans lequel vivaient les égyptiens permettait le développement rapide de maladies. Une simple projection dans les yeux de gouttes d'eau infectée peut provoquer une contamination. C’est donc pour ses vertus antibactériennes que la laurionite aurait été produite en grande quantité.
Un point sur nos défenses immunitaires
Les macrophages sont des cellules de défense qui empêchent la multiplication des bactéries à travers un mécanisme que l'on appelle phagocytose.
Ils ont pour but de détruire tout ce qu'ils ne reconnaissent pas comme faisant partie du soi. Outre le phénomène classique de reconnaissance antigène-anticorps, deux acteurs majeurs entrent en jeu dans le mécanisme de phagocytose : la NADPH-oxydase et la NO-synthase.
Maquillage et médecine
Le radical NO° possède, tout d’abord, des propriétés antibactériennes intrinsèques. Il est également produit par les macrophages et déclenche la lyse des cellules bactériennes phagocytées.
Un autre rôle majeur de NO° est la vasodilatation qui s'accompagne d'une augmentation de la perméabilité des vaisseaux et capillaires sanguins, permettant aux cellules le produisant de s'assurer un afflux sanguin important : les phagocytes peuvent donc affluer plus facilement dans ces régions. Cette production est stimulée par la présence d'ions calcium (Ca2+) mais il a été montré que les ions Pb2+ étaient confondus par les cellules avec cet ion. En effet, ces deux ions sont très semblables : même charge (+2), rayon ionique très semblable, même sphère de solvatation (6, 8 ou 10 molécules d'eau). Cette confusion est accentuée par le fait que notre organisme n'est pas naturellement exposé au plomb (ses composés étant généralement trop peu solubles) et ne sait pas sélectivement le reconnaître. Ces faits expliquent que l'exposition au plomb, même en faible quantité, soit toxique et provoque des maladies comme le saturnisme.
Le cas de la laurionite retrouvée dans les khôls est très différents de celui d'autres composés de plomb : dans le liquide lacrymal (pH ~ 2,7, [Cl-] ~ 0,1 mol.L-1), le diagramme de Pourbaix de la laurionite prévoit qu'à l'équilibre thermodynamique, dans ces conditions, la concentration en ions Pb2+ ne serait que de 10-4 mol.L-1. Cette valeur n'est qu'une borne maximale car, les quantités de khôl en contact direct avec le liquide lacrymal sont très faibles et le renouvellement constant de ce liquide ne permet pas d'atteindre cet équilibre. Les concentrations réelles ne seraient donc que micromolaires voire submicromolaires.
Dans ces conditions, il a été montré que la production de NO° par les kératinocytes (cellules de l'épiderme) est multipliée par trois ! L'affluence en macrophages due à la vasodilatation locale était donc assurée.
Note du photographe (en anglais): This is a lid for a canopic container in the shape of Tutankhamun's head. This 14th century BCE object was found in this young pharaoh's intact KV62 tomb from the 18th Dynasty of Egypt's New Kingdom and today forms part of the permanent collection of the Cairo Museum of Egypt. This photo was taken at the King Tut exhibition at the Pacific Science Center in Seattle, Washington State, USA.
Autrement dit, le maquillage des yeux par le fard noir chez les égyptiens leur assurait un liquide lacrymal enrichi de façon constante en ions Pb2+ et donc des yeux protégés en permanence par une riche population de macrophages constituant une barrière antibactérienne redoutable.
Conclusion
Le papyrus d'Ebers nous montre que la médecine égyptienne était très avancée et il est très probable que des observations empiriques leur aient permis de réaliser qu'un tel produit pouvait les protéger d'infections endémiques. Jusqu'à quel point étaient-ils conscients des véritables bienfaits du composé pour lequel ils ont mis en place une quasi-industrie très sophistiquée ?
Bibliographie et Ressources en Ligne
[1] Dioscoride, De Materia Medica, livre 5, 102; traduction : Georges Tsoucaris, C2RMF.
[2] C. Amatore. La chimie et l'art. EDP Sciences. p.60-95. 2010.
[3] P. Walter et coll., Nature, Vol 397, p 483 -484. 1999.
[4] P.Walter, C. Amatore et coll. Anal. Chem. 82, 457-460, 2010.
Remerciements
Cet article a été réalisé avec l'aide de Philippe Walter (directeur du Laboratoire d'Archéologie Moléculaire et Structurale, Sorbonne Université) et Christian Amatore (École Normale Supérieure, département de Chimie, Paris)