On appelle « carburants » les substances dont la combustion permet le fonctionnement des moteurs thermiques. L'énergie chimique contenue dans le carburant est donc destinée à être convertie en énergie mécanique. L'essence utilisée dans les voitures particulières est un cas particulier de carburant. Comme la plupart des carburants courants, l'essence est en fait un mélange de nombreuses espèces chimiques : plusieurs dizaines d'hydrocarbures « réservoirs d'énergie » et des additifs en faibles proportions introduits pour donner des propriétés particulières au mélange.
Les carburants
Qu'est ce qu'un carburant ?
On appelle « carburants » les substances dont la combustion permet le fonctionnement des moteurs thermiques. L'énergie chimique contenue dans le carburant est donc destinée à être convertie en énergie mécanique1. L'essence utilisée dans les voitures particulières est un cas particulier de carburant. Comme la plupart des carburants courants, l'essence est en fait un mélange de nombreuses espèces chimiques : plusieurs dizaines d'hydrocarbures « réservoirs d'énergie » et des additifs en faibles proportions introduits pour donner des propriétés particulières au mélange.
Les carburants les plus courants ainsi que leur usage et leur consommation annuelle en France sont donnés dans le tableau suivant.
| Carburant | Moteur | Consommation annuelle (France, Millions de tonnes Mt)2 |
|---|---|---|
| Essence | moteur à pistons : voitures particulières | 12 Mt |
| Gazole | moteur à pistons (diesel) : voitures particulières, véhicules de transport routier | 31 Mt |
|
Carburéacteur (« kérosène ») |
moteur à réaction3 : avions | 6 Mt |
| Carburants lourds (fiouls lourds) | moteur à pistons (diesel) : navires de moyen ou fort tonnage | 3 Mt |
Production des carburants par raffinage du pétrole
La principale voie d'obtention des carburants les plus courants est le raffinage du pétrole (on appelle « raffinage » l'ensemble des opérations visant à transformer le pétrole brut extrait du gisement en produits utilisables : combustibles, carburants, produits de base de l'industrie chimique...) [2-4].
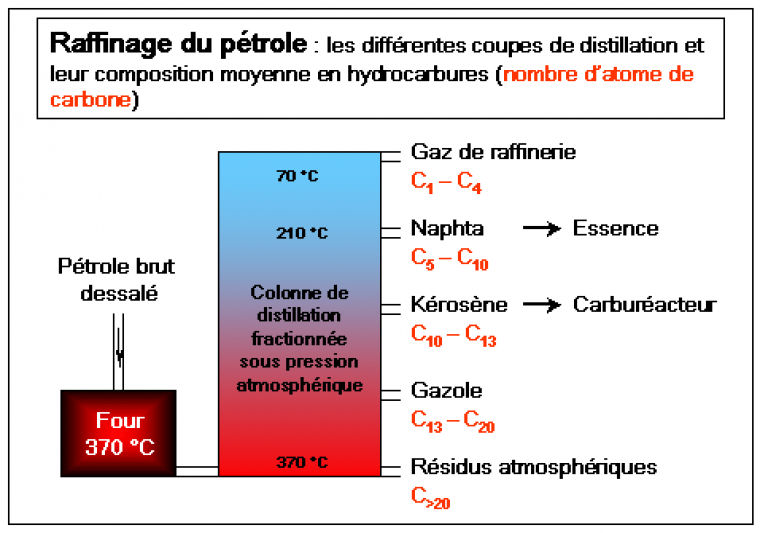
Le schéma suivant donne une vision simplifiée de la chaîne de raffinage : le pétrole brut contient toujours une certaine quantité d'eau salée, elle est extraite au cours de l'étape de dessalage. Il subit ensuite une séparation de ses constituants par distillation fractionnée sous pression atmosphérique [5]. Les colonnes utilisées peuvent atteindre soixante mètres de haut le long desquelles la température varie entre 370 et 70 °C. Elles sont conçues pour que les produits puissent être retirés à différentes hauteurs; on parle des « coupes de distillation ».
Les différentes coupes de distillation prélevées le long de la colonne sont :
-
En fond de colonne : les hydrocarbures les plus lourds (C > 20, à plus de 20 atomes de carbone par molécule), appelés « résidus atmosphériques ». Ce sont ceux dont le point d'ébullition est le plus élevé. Pour subir une séparation plus poussée, ils doivent être distillés sous vide.
-
La température d'ébullition du mélange décroît avec sa hauteur dans la colonne et on sépare les gazoles (C13-C20), le kérosène (C10-C13), matière première du carburéacteur, puis le naphta (C5-C10), qui permettra de produire les essences ordinaires et super.
-
En tête de colonne, on récupère les produits les plus volatils à l'état gazeux (C1-C4).
À titre d'exemple, la plus grosse raffinerie de France (raffinerie de Normandie, groupe Total) a une capacité de distillation de 16 millions de tonnes de brut par an.
Les autres filières de production : la synthèse de Fischer-Tropsch
D'autres filières permettent de produire des carburants par voie synthétique. Elles reposent toutes sur le procédé Fischer-Tropsch mais diffèrent par la matière première utilisée (la « charge »). En effet, la nature exacte de la charge n'est pas primordiale, le seul impératif est qu'elle doit être riche en carbone et en hydrogène. Les procédés les plus répandus utilisent :
-
Le gaz naturel : ce procédé appelé GTL (« Gas To Liquid ») est le procédé Fischer-Tropsch historique (1923). Les carburants obtenus restent encore chers devant ceux provenant du raffinage pétrolier, mais le procédé est l'objet de développement visant à améliorer sa rentabilité.
-
Le charbon : procédé utilisé jusque dans les années 1990 puis abandonné en raison de sa faible rentabilité.
-
La biomasse, c'est à dire les huiles végétales (colza), les céréales (blé, maïs) et les plantes sucrières (betteraves). Ce procédé permet d'obtenir des « biocarburants ». S'ils sont pour l'instant peu compétitifs par rapport aux carburants issus de la filière pétrole, ils présentent l'avantage d'exploiter des ressources renouvelables, contrairement aux combustibles fossiles (pétrole, gaz naturel et charbon). On peut également envisager l'utilisation de déchets agricoles, ménagers ou industriels.
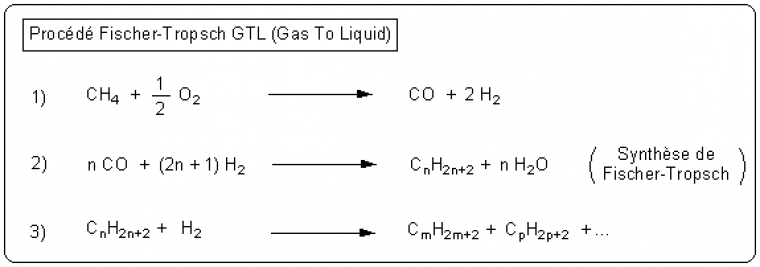
Ces trois procédés reposent sur la même chaîne réactionnelle développée dans la figure ci-dessous sur l'exemple du gaz naturel :
-
La charge subit un vaporéformage (une gazéification dans le cas du méthane) qui permet de la transformer en « gaz de synthèse » : un mélange CO + H2.
-
Le gaz de synthèse est transformé en hydrocarbures paraffiniques1 sous l'action d'un catalyseur. Cette étape (synthèse de Fischer-Tropsch) est au coeur du procédé de chaque filière, quelle que soit la charge de départ.
-
Les hydrocarbures formés subissent un hydrocraquage qui permet l'obtention des carburants classiques.
Composition et combustion de l'essence
Composition de l'essence
Les carburants usuels n'ont pas une composition bien définie. Ce sont des mélanges d'hydrocarbures qui varient avec l'origine géographique du pétrole utilisé et les procédés de raffinage appliqués. En fait le mélange ne peut être commercialisé que s'il vérifie des contraintes très strictes sur les propriétés physiques (densité, volatilité) énergétiques (pouvoir calorique) et chimiques (indice d'octane, limitation des teneurs en certains composants).
Par exemple, pour être vendu sous l'appellation eurosuper (super 95), un mélange doit avoir une densité comprise entre 0,72 et 0,78 kg/L à 15 °C et un indice d'octane2 de 95 au moins. La composition du mélange doit vérifier une dizaine de valeurs limites. Par exemple, la quantité de benzène en volume doit être inférieure à 1 %, celle de soufre inférieure à 150 mg/kg, celle de plomb inférieure à 5 mg/L [6].
Les essences usuelles (super 95 et 98) et le gazole sont des mélanges de plusieurs dizaines d'hydrocarbures (alcanes linéaires et ramifiés, alcènes, aromatiques) auxquels on a ajouté des additifs qui apportent des propriétés particulières : éthers (amélioration de l'indice d'octane), détergents et surfactants (lutte contre les phénomènes d'encrassement du moteur), colorants etc. Pour déterminer les propriétés énergétiques de ces carburants, on les modélise par un « hydrocarbure moyen » : l'octane C8H18 pour l'essence et le dodécane C12H26 pour le gazole.
Combustion de l'essence
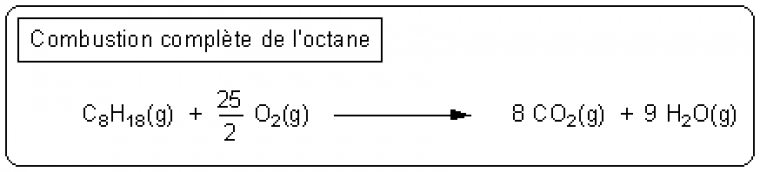
Dans un moteur, c'est la réaction de combustion de l'essence qui dégage l'énergie nécessaire au fonctionnement. Dans le cas de l'octane, choisi pour modéliser le mélange d'hydrocarbures constitutif de l'essence, le bilan de la combustion complète par le dioxygène est le suivant :
L'enthalpie standard de réaction, ΔrH°, de cette combustion est de l'ordre de -5000 kJ/mol : elle est donc très exothermique. Ceci montre qu'une grande quantité d'énergie est disponible, stockée sous une forme chimique dans le carburant.
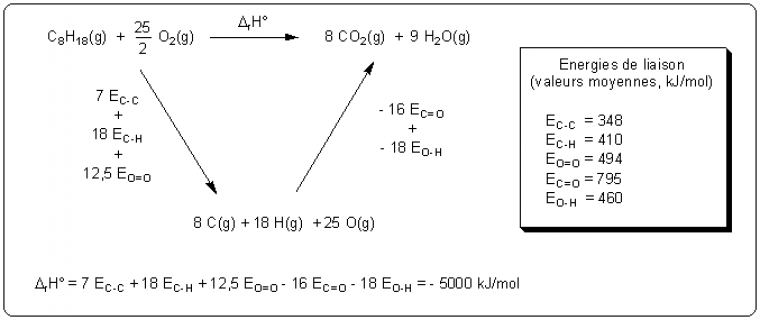
Cette énergie est libérée principalement au cours du réarrangement des liaisons chimiques. Les liaisons C-C, C-H et O=O sont brisées pour former des liaisons C=O et O-H. Le cycle thermodynamique ci-dessous permet de retrouver la valeur de ΔrH°.
Dans la pratique, l'essence est caractérisée par son Pouvoir Calorifique, PC, qui est la quantité d'énergie libérée par la combustion complète d'une masse d'un kg. PC = -ΔrH°/M où M est la masse molaire de la substance considérée. Dans le cas de l'octane, PC(octane) = 44.103 kJ/kg. On constate que cette valeur est très proche de celle obtenue expérimentalement pour les essences réelles, cela justifie a posteriori le choix de l'octane pour modéliser l'essence. Le pouvoir calorifique du gazole est légèrement inférieur à celui de l'essence.
Rendement d'un moteur usuel
Même dans des conditions d'utilisation optimales (travail à pleine charge), le rendement des moteurs à essence ne dépasse pas 36 % (42% pour le diesel) [7]. Le reste de l'énergie est dissipée en chaleur. Pour une utilisation à charge réduite (courts trajets en ville par exemple), le rendement devient inférieur à 15 %. C'est pourquoi les moteurs sont encore aujourd'hui l'objet de nombreuses recherches visant à optimiser leur fonctionnement.
Conclusion et perspectives
Il est clair que l'utilisation des combustibles fossiles pour produire les carburants usuels n'est pas une solution durable. L'épuisement des réserves à plus ou moins long terme est aujourd'hui admis (cf l'article « Les combustibles fossiles : formation, composition et réserves ») et la migration vers d'autres sources de production ou d'autres carburants semble inéluctable. De plus, l'utilisation des carburants issus des combustibles fossiles n'est pas sans conséquences sur l'environnement et la santé. En effet, la combustion de ces carburants entraîne l'émission de nombreuses substances polluantes :
-
Le CO2, qui est avec l'eau le principal produit de la combustion complète des carburants. C'est un gaz à effet de serre : son rejet dans l'atmosphère favorise le réchauffement climatique.
-
Le monoxyde de carbone CO et les hydrocarbures imbrûlés (HC) dont le benzène, qui sont émis lorsque la combustion du carburant dans le moteur est incomplète. Ces substances sont dangereuses pour la santé humaine.
-
Les oxydes d'azote NOx qui sont formés par réaction entre le diazote et le dioxygène de l'air dans la chambre de combustion. Ils peuvent générer des pluies acides et participent à la formation de l'ozone atmosphérique qui entraîne des pics de pollution.
Les efforts à court terme sont concentrés sur l'amélioration des performances des moteurs et des systèmes de post-traitement. Par exemple, une optimisation des processus de combustion par injections multiples permet d'augmenter le rendement du moteur et de réduire les émissions de polluants de combustion incomplète (CO et HC). D'autre part, les émissions des polluants formés sont réduites par l'utilisation de pots catalytiques trois voies qui permettent simultanément l'oxydation de CO et des HC en CO2 et la réduction des NOx en N2[8].
À plus long terme, des changements de technologie sont envisagés avec la migration vers de nouveaux systèmes de motorisation et de nouvelles sources d'énergie :
-
Moteur dédié au gaz naturel :
Le méthane, principal constituant du gaz naturel, est, comme le pétrole, un combustible fossile non renouvelable. En revanche, sa combustion émet moins de CO2 et moins de polluants que l'essence et le diesel, à énergie fournie égale. C'est donc un carburant intrinsèquement plus « propre ».
-
Moteur hybride thermique/électrique :
Le moteur thermique classique est couplé à un moteur électrique qui n'émet aucun polluant. L'énergie électrique peut éventuellement provenir d'une source non-fossile. Lors du freinage, le moteur fonctionne en générateur électrique ; il est couplé à une batterie / un accumulateur fonctionnant en récepteur électrochimique, ce qui permet la récupération d’énergie.
-
Moteur à pile à combustible :
L'énergie provient de la réaction de formation de l'eau par oxydoréduction entre le dihydrogène et le dioxygène. L'énergie chimique est dans ce cas transformée en énergie électrique avant d'être convertie en énergie mécanique. Son fonctionnement s'accompagne d'émission de polluants très faible par rapport à celles des moteurs thermiques actuels.
On peut également envisager le remplacement des carburants actuels par des biocarburants qui peuvent être des hydrocarbures ou bien d'autres substances (éthanol, esters...). Ils sont synthétisés à partir de la biomasse par le procédé Fischer-Tropsch s'il s'agit d'hydrocarbures (cf les autres filières de production) ou bien par d'autres procédés, éventuellement biochimiques (catalyse enzymatique). L'avantage à long terme de la biomasse est de constituer une source d'énergie renouvelable, elle permet donc un développement soutenable1.
Bibliographie et ressources en ligne
Données sur la consommation, statistiques
[1] Chiffres et statistiques sur la production et la consommation des énergies en France sur le site de la Direction Générale de l'Énergie et des Matières Premières.
Les procédés utilisés en chimie industrielle
[2] R. Perrin, J-P. Scharff « Chimie Industrielle » 2ème éd. 1997 Dunod.
[3] K. Weissermel, H-J. Arpe « Chimie organique industrielle », 2000, DeBoeck.
[4] Le raffinage industriel sur le site de l'Institut Français du Pétrole.
[5]La distillation fractionnée sur le site CultureSciences-Chimie
Moteur thermique - pot catalytique
[7] Le fonctionnement d'un moteur thermique sur le site de l'Institut Français du Pétrole.
[8] Chimie du pot catalytique: principe, enjeux et polémique sur CultureSciences-Chimie.
Biocarburants
[9] Les biocarburants : de la 1ère à la 3ème génération ! sur CultureSciences-Chimie.