Les changements d'état sont largement utilisés dans toutes les étapes de séparation et de purification. La distillation, et plus particulièrement l'hydrodistillation, est une technique basée sur le changement d'état liquide - vapeur des espèces chimiques.
Introduction
Les changements d'état sont largement utilisés dans toutes les étapes de séparation et de purification. La distillation, et plus particulièrement l'hydrodistillation, est une technique basée sur le changement d'état liquide - vapeur des espèces chimiques.
La séparation de deux phases liquides non miscibles est relativement aisée par simple décantation. Il est cependant plus compliqué de séparer un composé d'un mélange complexe. Cette séquence présente l'hydrodistillation, technique se basant sur la distillation d'une solution aqueuse contenant un composé organique non miscible à l'eau, ici le limonène.
Présentation du matériel
Nous avons ici besoin de ces différents éléments :
-
bain d'huile et plaque chauffante magnétique (ou chauffe-ballon, avec agitation magnétique),
-
support élévateur,
-
ballon bicol de 2 L,
-
2 thermomètres rodés,
-
adaptateur (si nécessaire) (tête de colonne),
-
réfrigérant à eau coudé (ou réfrigérant à eau + allonge coudée) et tuyaux,
-
éprouvette graduée de 250 mL
-
puissant barreau aimanté
-
potence, noix et pinces
-
écorces de 4 oranges
-
un entonnoir à solide
Mise en place du matériel
Au préalable, on a bien pris soin de graisser tous les rodages mâles. La plaque chauffante magnétique et le bain d'huile sont placés sur le support élévateur en position basse. Le ballon est fixé à la potence à l'aide d'une noix et d'une pince à une hauteur telle que l'on puisse retirer le moyen de chauffage lorsque le support est en position basse. On place sur le premier col, la tête de colonne avec un thermomètre et le réfrigérant coudé et, sur le deuxième col, un bouchon rodé. Notons que le réfrigérant à eau coudé est relié directement au ballon. Il est totalement inutile d'insérer une colonne de séparation (type Vigreux par exemple) entre les deux. L'éprouvette est placée sous l'extrémité du réfrigérant coudé.
Réalisation de l'expérience
On enlève le bouchon, puis on introduit, à l'aide d'un entonnoir, les écorces d'orange (coupées en petits morceaux, partie blanche située entre le zeste et les quartiers d'oranges exclue) et de l'eau distillée à environ la moitié de sa hauteur. Le thermomètre et le clip sont ensuite replacés. Le bain d'huile est monté au contact du ballon et la plaque chauffante est mise en marche. On vérifie que l'eau circule bien dans le réfrigérant.
On observe au bout d'une dizaine de minutes la condensation de vapeurs dans le réfrigérant. Après environ 30 minutes de distillation, on récupère dans l'éprouvette un mélange biphasé constitué d'eau (phase inférieure) et de limonène (phase supérieure). Le limonène peut alors être séparé de l'eau par décantation.
|
|
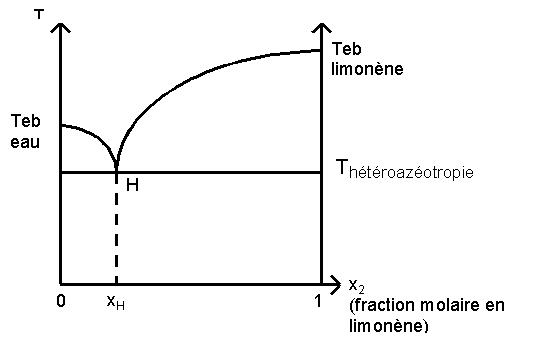
Le diagramme binaire eau/limonène présente un hétéroazéotrope [2] à la composition xH en limonène. La vapeur dégagée a donc cette composition tant que du limonène est présent en solution, puis est constituée d'eau pure lorsque tout le limonène a été distillé, en effet dans notre cas la fraction molaire en limonène est inférieure à xH. L'eau et le limonène étant non miscibles, le distillat est biphasique et la séparation est facile. On peut alors se demander pourquoi il était insuffisant de se contenter d'une décantation sur le mélange initial. La réponse tient au fait que, même si on a représenté ici un mélange binaire, la solution initiale était constituée de nombreux composés que l'on n'a pas considérés. Ces composés ne formant pas d'hétéroazéotropes avec l'eau, ils ne seront pas entraînés avec la vapeur d'eau. Cependant, la température d'ébullition n'est pas celle d'hétéroazéotropie TH à cause de la présence de ces composés.
Conclusion
La technique d'hydrodistillation permet d'obtenir, à partir d'un mélange complexe, le composé organique souhaité par simple séparation de phases dès lors que ce dernier est non miscible à l'eau. L'avantage principal de cette méthode par rapport à une distillation fractionnée tient aux températures utilisées : l'hétéroazéotrope est distillé à des températures, TH, toujours inférieures à 100 °C, alors que les températures d'ébullition de nombreux composés organiques sont nettement supérieures à cette valeur. Ceci explique que cette technique est très largement utilisée en parfumerie, où les molécules odorantes sont souvent fragiles et ne peuvent supporter des températures importantes.
Une variante de cette technique consiste à apporter de la vapeur d'eau de l'extérieur et non pas à chauffer le ballon contenant les composés à récupérer. On parle alors d'entraînement à la vapeur.
Notons enfin que ce principe peut être mis à profit afin d'éliminer l'eau d'un mélange réactionnel, par exemple en utilisant un montage de Dean-Stark.
Références bibliographiques pour approfondir
[1] M. Capon. V. Courilleau-Haverlant. C. Valette. Chimie des couleurs et des odeurs. Cultures et Techniques - Nantes. 1993.
[2] M. Chavanne. G. J. Beaudouin. A. Jullien. F. Flammand. Chimie organique expérimentale. Ed. Modulo. 1991.