Cet article présente la microscopie à force atomique (AFM) et quelques-unes de ses applications.
La microscopie à force atomique (ou AFM pour Atomic Force Microscopy), inventée en 1986 par les chercheurs d’IBM Gerd Binnig, Calvin Quate et Christoph Gerber (Figure 1), est un type de microscopie à sonde locale à très haute résolution. Son précurseur, le microscope à effet tunnel (ou STM pour Scanning Tunneling Microscopy), inventé en 1981 par Gerd Binnig et Heinrich Rohrer, fut récompensé par le prix Nobel de physique en 1986.
L’AFM permet d'analyser une surface point par point grâce à un balayage par une sonde constituée d’une pointe fine, ce qui constitue sa différence principale avec les microscopes usuels et en fait un outil remarquable pour l’observation d’objets à très petite échelle. Depuis leur développement au cours du 17ème siècle, les microscopes optiques ont bénéficié des avancées technologiques en matière notamment de fabrication de lentilles afin de repousser toujours plus loin les limites de l’observation à petite échelle. L’observation directe des objets grâce à la lumière fait la force principale de la microscopie optique, mais c’est également sa plus grande faiblesse. À l’échelle où les objets atteignent une taille proche de la longueur d’onde de la lumière incidente apparaissent des phénomènes de diffraction qui rendent l’observation de détails de moins de quelques centaines de nanomètres difficile.
En n’utilisant pas la lumière comme moyen direct d’observation, l’AFM permet de s’affranchir des limites posées par la diffraction et d’avoir accès à un niveau de détail jusqu’alors inégalé. Cette technique connaît un franc succès depuis son développement, et notamment auprès des chimistes. Le nombre de publications sur le sujet a connu un essor phénoménal dans les années 2000 et continue toujours d’augmenter (Figure 2).
Contrairement à la spectroscopie, l’AFM permet au chimiste de réellement voir les objets sur lesquels il travaille. Il est ainsi désormais possible d’observer des détails compris entre quelques dixièmes de nanomètres et une dizaine de micromètres (cela dépend de l’échelle à laquelle la pointe balaye l’échantillon).
Principe général
Principe de base
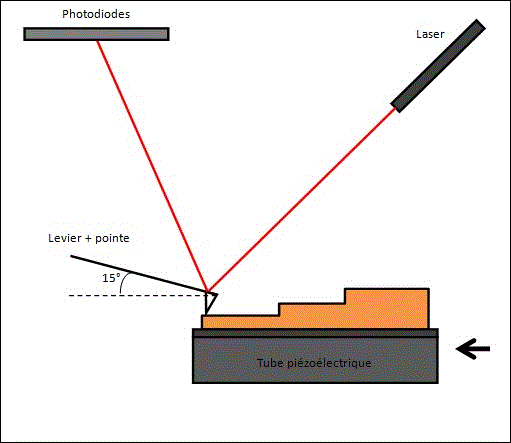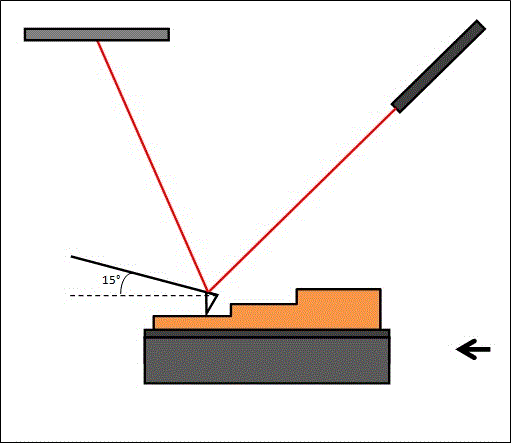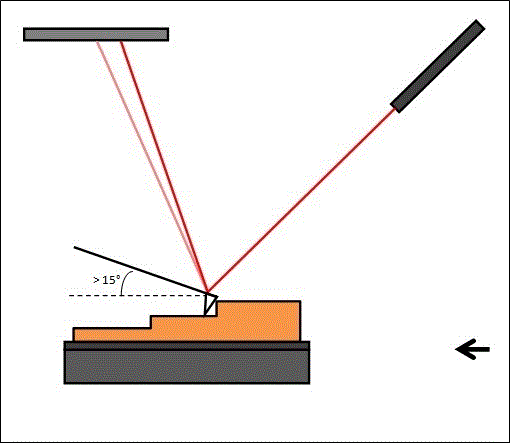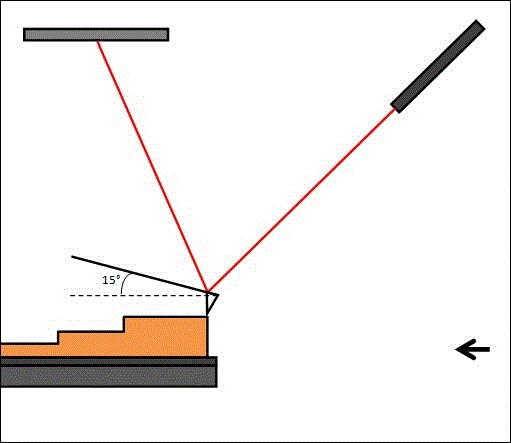
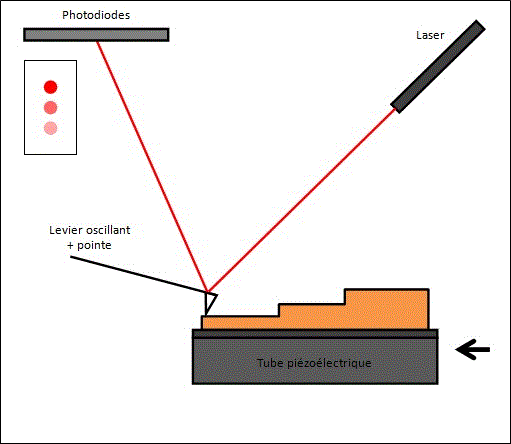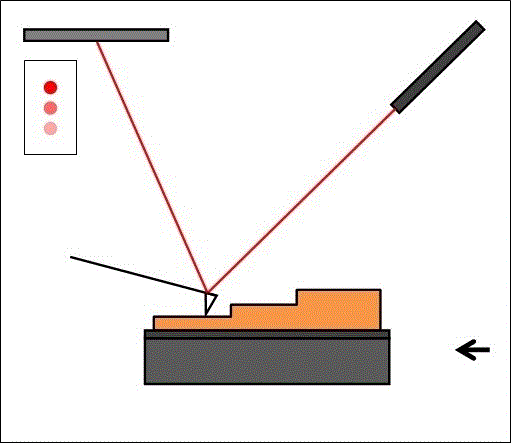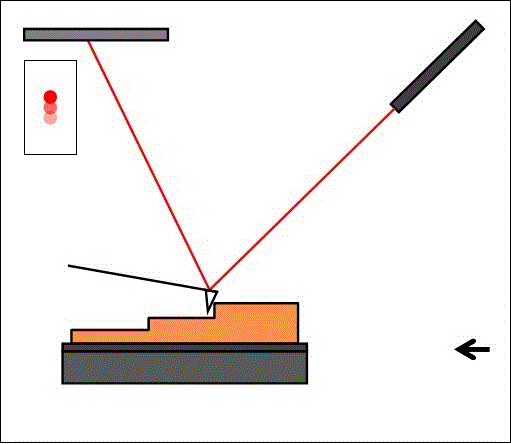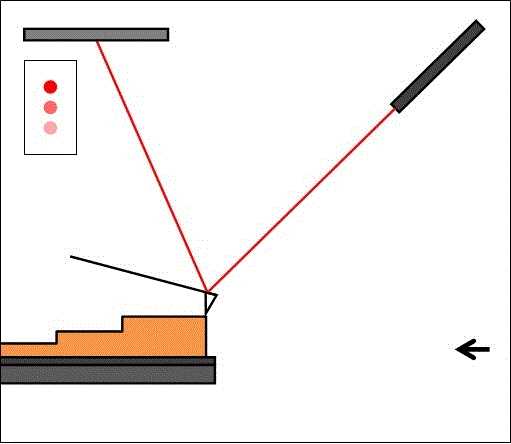
L’AFM permet d'analyser une surface point par point grâce à un balayage par une sonde. Cette dernière est constituée d’une pointe très fine, positionnée à l'extrémité d'un micro-levier flexible. Ce type de microscopie fonctionne en mesurant l'interaction attractive ou répulsive entre les atomes constituant la pointe nanométrique et les atomes surfaciques d'un échantillon. Quand la pointe est à proximité d’une surface, les forces d’interactions entre la pointe et l’échantillon entraînent une déviation du levier qui suit la loi de Hooke.
L'analyse de la déviation du levier, à l’aide d’un laser, permet à la fois de déterminer le parcours exact de la pointe et de mesurer les forces d’interactions entre cette dernière et l’échantillon (Figure 3).
Appareillage
Les microscopes à force atomique sont composés de 3 parties principales :
Le levier et la pointe
Le levier de l’AFM est une pièce flexible sur laquelle est fixée la pointe d'analyse et dont la face supérieure permet de réfléchir le faisceau laser vers le détecteur.
La pointe est la partie de l’appareil en contact permanent ou périodique avec l'échantillon.
La résolution du microscope dépend principalement de la taille de l'apex nanométrique de la pointe. Plus l'apex sera petit, plus la résolution sera élevée. En pratique, on obtient une résolution maximale quand la pointe est fonctionnalisée avec une molécule diatomique linéaire comme le monoxyde de carbone (CO), ce qui permet d'avoir un apex monoatomique (Figure 4).
La pointe est souvent en nitrure de silicium Si3N4 ou en silicium sous forme de pyramide (Figure 5).
Les tubes piézoélectriques
Un premier tube piézoélectrique permet de déplacer l’échantillon dans les trois directions de l’espace. Les céramiques piézoélectriques sont des matériaux qui se contractent ou s’étirent en présence d’un gradient de tension électrique. En pratique, quatre électrodes sont placées sur la surface extérieure du tube sur lequel est placé l’échantillon tandis qu’une électrode unique couvre l’intérieur (Figure 6) : appliquer une tension sur une ou plusieurs électrodes entraîne la contraction ou l’étirement du tube, ce qui met en mouvement le support de l’échantillon (ou du levier). Les électrodes extérieures permettent les mouvements dans les directions xy, l’électrode interne le mouvement dans la direction z. En outre, un autre tube piézoélectrique permet les mouvements du levier.
Tout comme la taille de l’apex nanométrique, la réponse mécanique du tube piézoélectrique à la contrainte de tension a une influence sur la résolution du microscope.
Le détecteur photodiode
Afin de pouvoir observer la déviation du levier et la traduire en signal, les AFM sont équipés de photodiodes sur lesquelles va se refléter le rayon laser.
L’AFM en fonctionnement
La mesure de la déviation
Plusieurs méthodes permettent d’analyser la déviation du levier balayant l’échantillon. Typiquement, la déviation est mesurée à l’aide d’un rayon laser qui se réfléchit sur la surface du levier et qui est ensuite détecté par une photodiode circulaire divisée en quadrants, qui traduit le signal lumineux en tension électrique.
Si le levier s’infléchit à cause des forces d'interactions, le faisceau laser est dévié et la position détectée par les photodiodes varie. Quand le faisceau n'est pas dévié, il frappe au centre du détecteur et illumine les 4 photodiodes de manière égale. Si le faisceau laser est dévié, certaines photodiodes recevront plus de lumière que d’autres : il apparaît alors une différence de tension directement liée aux forces d’interaction et à la hauteur de l’échantillon (figure 7).
La mesure par laser est non seulement facile à mettre en œuvre, mais permet également d’avoir accès de façon qualitative à la nature chimique de la surface. En effet, le contact entre la pointe et la surface génère des frottements : le levier subit une torsion autour de son axe, ce qui induit une différence de tension non plus entre le haut et le bas du quadrant, mais entre sa droite et sa gauche.
Rétroaction
Si la pointe balaie la surface à hauteur constante, elle risque d’être endommagée ou d’endommager l’échantillon : il existe donc un système de rétroaction qui permet d’ajuster la distance entre la pointe et l’échantillon (figure 8).
Le circuit de rétroaction ajuste la tension appliquée au tube piézoélectrique pour déplacer l’échantillon et ainsi maintenir une distance constante entre la pointe et l'échantillon.
Les différents modes de fonctionnement
Depuis la création de l’AFM, différents mode d’utilisation de l’appareil ont été développés. Nous détaillons les trois plus courants :
- Le mode contact utilise les forces répulsives. La pointe appuie légèrement sur la surface, elle est donc repoussée du fait du principe de Pauli et le levier est infléchi. L’appareil mesure alors la déviation, ce qui donne accès à la hauteur de l’échantillon et permet d’effectuer la rétroaction (Figure 9). En pratique, le signal de rétroaction est souvent utilisé pour garder le levier à une position constante.
- Le mode contact intermittent ou tapping est le plus utilisé : il s’agit de faire vibrer le levier à sa fréquence propre de résonance (de l'ordre de 50-100 kHz), avec une certaine amplitude. Lorsque la pointe interagit avec la surface, l'amplitude d'oscillation du levier diminue (Figure 10). L’appareil mesure cette différence d’amplitude, ce qui permet d'obtenir des informations sur l'échantillon à analyser comme sa hauteur locale par exemple. Un rétrocontrôle est ensuite effectué pour ajuster la hauteur de l’échantillon et poursuivre les mesures afin de minimiser l’usure de la pointe.
- Le mode non contact ou modulation de fréquence utilise les forces attractives. La pointe ne touche pas l’échantillon et le levier oscille avec une fréquence proche ou égale à sa fréquence de résonance. La pointe est gardée à une distance fixe de l’échantillon et la déviation du levier n’est due qu’aux interactions attractives entre la pointe et l’échantillon. C’est un mode de fonctionnement essentiellement utilisé sous vide.
Utilisations courantes
L'un des principaux domaines d’application de l’AFM est l’observation de surfaces nues ou sur lesquelles sont adsorbés des objets d’intérêt. La résolution que l’on peut obtenir avec cette technique permet d’observer des détails à une échelle encore jamais égalée.
La catalyse fait partie des domaines dans lesquels la connaissance exacte de la structure de la surface est d’une importance capitale. Cela permet de comprendre le fonctionnement des catalyseurs et d’améliorer leur synthèse afin d’en augmenter le rendement par exemple. Un exemple de ce type d’application a été donné dès 1995 par l’équipe de Naoichi Yamamoto à Tokyo (Japon) dans un article intitulé « Using Atomic Force Microscopy to Image the Surface of the Powdered Catalyst KMn8O16 » publié dans la revue Journal of Catalysis (Journal of Catalysis 159, 401–409 (1996)). L’équipe japonaise s’est intéressée à l’étude de catalyseurs solides à base d’oxyde de magnésium KMn8O16, qui sont utilisés notamment en catalyse d’oxydoréduction, mais aussi en catalyse acido-basique (oxydation et hydratation, des nitriles aux amides). Les mécanismes de ces réactions ne sont cependant pas encore bien connus et des informations structurales sur le catalyseur (comme la répartition des sites acido-basiques ou d’oxydation) sont nécessaires pour les élucider. Du fait qu’il est très difficile d’obtenir des monocristaux de KMn8O16 pour résoudre leur structure par diffraction des rayons X, l’AFM est un outil de choix pour obtenir ce genre d’informations. Les analyses ont en effet montré que la poudre de catalyseur analysée était constituée de fines aiguilles dont la surface était composée de facettes (ce qui expliquerait la grande surface active du catalyseur : 123 m²/g), et que chaque facette avait une structure en rainures fines. Les auteurs ont par la suite pu établir un modèle de la structure de la surface du catalyseur à partir des images AFM obtenues. Sans pour autant obtenir une observation détaillée de chaque atome à la surface du catalyseur, cette étude a tout de même permis d’obtenir des informations précieuses à son sujet.
L’observation d’objets adsorbés sur une surface plane est également une des applications principales de l’AFM. Qu’il s’agisse de feuillets de graphène, de molécules organiques ou de nano-objets, le niveau de détail atteint par cette technique est phénoménal. En 2006 par exemple, Paul Rothemund, un chercheur de l’université Caltech, publie un article dans la célèbre revue Nature où il présente un concept de fabrication de nano-objets à partir de brins d’ADN repliés de mille et une façons à la manière d’un origami afin d’obtenir une forme pré-déterminée (Nature 440, 297-302 (2006)). L’aspect très conceptuel de l’article concernant les séquences d’ADN à utiliser et la torsion des brins est vite balayé par la présentation d’images obtenues par AFM d’objets ayant des formes aussi diverses qu’étonnantes. La taille typique de ces objets (environ 100 nm x 100 nm, Figure 11) rend leur observation par AFM tout à fait indiquée.
Dans cette étude, les objets appelés « Origamis d’ADN » sont adsorbés sur une surface fraichement clivée de mica. Le mica sous cette forme est connu pour avoir une surface très plane et très propre, ce qui permet d’éviter toute pollution de l’échantillon et de ne pas le déformer (par adsorption sur une surface avec des bosses par exemple).
Les exemples développés ici ne constituent pas une liste exhaustive des applications de la microscopie à force atomique. L’augmentation de la précision des tubes piézoélectriques et la diminution de la taille de l’apex nanométrique de la pointe ont permis à de nombreuses équipes dans le monde de repousser encore plus loin les limites de l’observation du nano-monde.
Application au suivi d’une réaction chimique
La microscopie à force atomique est utilisée en physique, en chimie mais également en biologie, notamment pour l’étude des interactions ADN-protéines. En 2013, une autre application particulièrement intéressante a été développée.
Que se passe-t-il au niveau atomique lors d’une réaction chimique ? Des modèles ont permis de décrire les mécanismes, mais la plupart du temps, il est difficile de suivre expérimentalement les réarrangements mis en jeu. Une équipe de physiciens et de chimistes de l’université de Berkeley en Californie présente une toute nouvelle application de la microscopie à force atomique : l’observation de molécules avant et après une réaction (Figure 12). Grâce à cette technique, les chercheurs ont pu obtenir des « photos » de molécules carbonées où l'on peut distinguer les atomes de carbones des liaisons covalentes, ce qui permet d’observer directement les modifications de la structure de la molécule au cours de la réaction. Jusqu’alors, seule une analyse spectroscopique permettait d’obtenir ce genre d’informations. Les enjeux sont donc énormes : outre la possibilité de voir les molécules telles qu’elles sont, ce qui est en soi une avancée à la fois du point de vue pédagogique et comme confirmation de la structure exacte de la molécule, il sera possible de mieux cibler les modifications à effectuer pour optimiser une réaction particulière. Les chercheurs font d’ailleurs remarquer que les produits obtenus n’étaient pas nécessairement ceux qu’ils avaient prévus. En effet, la réaction donne majoritairement deux produits de cyclisation alors que de nombreux autres produits auraient pu être prédits.
Leur article a été cité à plusieurs reprises depuis sa parution et ce procédé largement réutilisé, notamment pour des réactions de polymérisation. Ainsi, dans un autre article (Science 340, 1434 (2013)), l’AFM est utilisée pour étudier des réactions de formation de polymères. Sur la Figure 13, on observe distinctement les deux conformères cis et trans du précurseur 1. Ce dernier peut ensuite donner le monomère 2, via une cyclisation C1-C5 ènediyne qui conduira à une réaction de polymérisation selon un mécanisme radicalaire.
Grâce à la microscopie à force atomique, il est possible d’observer non seulement l’oligomère, mais aussi des polymères de différentes tailles et d’autres petites molécules (Figure 14).
Le développement de cette technique apparaît fondamental et révolutionnaire. D’ailleurs, les chercheurs ne cachent pas leur enthousiasme :
« Être capable de voir ces images m'a bluffé ! », a déclaré le chercheur qui a dirigé les recherches, Felix Fischer, « Mes professeurs disaient que nous ne pourrions jamais le voir réellement, et pourtant nous l’avons maintenant sous les yeux. »
Effectivement, il y a vingt ans encore qui aurait pu imaginer que nous serions en mesure d'obtenir des images aussi précises de ce qui se passe à l'échelle moléculaire ? Pouvoir distinguer les différents atomes d'une molécule et en avoir une image presque nette fait partie du rêve de tout chimiste.
La prochaine étape pourrait être de distinguer les différents atomes sur de telles images ou encore d'être capable d'observer les atomes d'hydrogène plus distinctement.
Quoiqu’il en soit, les perspectives de développement de cette technique sont multiples et passionnantes, et le moins qu’on puisse dire, c’est que cela devrait aider à rendre la chimie moins abstraite !
Bibliographie
- Afm Express. Guide Pratique pour la Microscopie a Force Atomique - Exploration du Nanomonde, G. Francius, (2011) Presses Universitaires de Nancy.
- Atomic Force Microscopy: Understanding Basic Modes and Advanced Applications, G. Haugstad, (2012) John Wiley & Sons, Inc.
- Dimas G. de Oteyza et al. Science 340, 1434 (2013).
- http://pubs.acs.org/doi/abs/10.1021/nl403791q
- http://newscenter.lbl.gov/news-releases/2013/05/30/atom-by-atom/ consulté le 14 avril 2014.
- http://fr.wikipedia.org/wiki/Microscope_à_force_atomique consulté le 27 mars 2014.
- Atomic Force Microscopy: General Concept and Defining Characteristics, http://www.nrl.navy.mil/chemistry/6170/6177/afm_concept.php consulté le 22 avril 2014.
- http://virtual.itg.uiuc.edu/training/AFM_tutorial/ consulté le 25 avril 2014
- Naoichi Yamamoto et al. Journal of Catalysis 159, 401-409 (1996).
- Paul W. K. Rothemund Nature 440, 297-302 (2006).