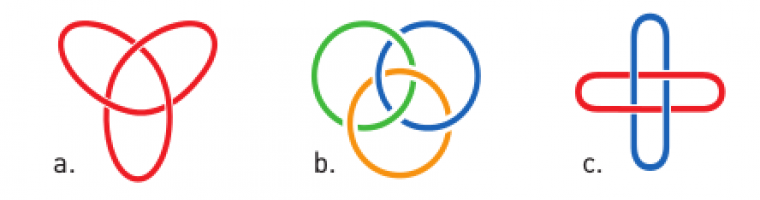Le Prix Nobel de Chimie 2016 a été attribué à Jean-Pierre Sauvage, Sir James Fraser Stoddart et Bernard L. Feringa pour leurs travaux de recherches sur le développement de machines moléculaires.
Introduction
Richard FEYNMAN, prix Nobel de physique en 1965, avait prévu dès les années 1960 le développement des nano-technologies. En 1984, lors d'une conférence visionnaire, il évoque publiquement sa conviction de la possibilité, un jour, de construire des machines à l'échelle moléculaire. Il sait que ces « machines moléculaires » existent dans la nature : par exemple le flagelle de certaines bactéries, macromolécule en forme de tire-bouchon, permet à celles-ci de se mouvoir. Jean-Pierre Sauvage, Sir James Fraser Stoddart et Bernard L. Feringa ont montré, par leurs travaux, qu'il était possible de concevoir et de synthétiser ces « machines moléculaires ». De même que le XIXème siècle a vu naître, avec le progrès technique et l’élaboration de machines (à l’échelle humaine), la révolution industrielle, nous sommes sans doute à l'aube d'une autre révolution.
Mais qu'entend-t-on exactement par « machine moléculaire » ? Il s'agit d'un assemblage de composants moléculaires distincts, conçu pour effectuer des mouvements comme une machine, sous l'effet d'un stimulus extérieur et via un apport d'énergie.
On peut distinguer deux approches dans leur conception: la première consiste à enchevêtrer des molécules les unes dans les autres (c'est l'approche de Jean-Pierre Sauvage et de James Fraser Stoddart) et la seconde à utiliser les liaisons multiples pour concevoir des moteurs moléculaires (c’est celle de Bernard L. Feringa).
Entrelacer des molécules les unes dans les autres
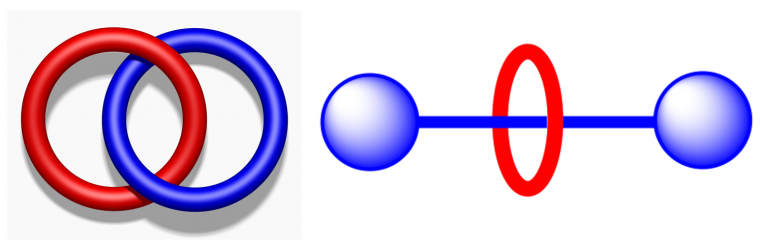
Il s'agit d'enchevêtrer des molécules les unes dans les autres, via des liaisons mécaniques et non covalentes: par exemple, deux molécules en forme d’anneaux peuvent être imbriquées l'une dans l'autre (structure de type caténane, du latin catena, qui veut dire chaîne) ou bien une molécule en forme d’anneau peut être « enfilée » sur une molécule en forme d'axe, comme une perle sur un fil (structure de type rotaxane). Ledit fil est muni de « bouchons » (en pratique, des groupements volumineux) à ses extrémités pour éviter que la molécule jouant le rôle de perle ne s’échappe (Figure 1).
Les différentes parties peuvent se mouvoir de façon indépendante l’une de l’autre, dans une certaine mesure : dans un [2]catenane, un anneau peut tourner à l’intérieur de l’autre. Dans un [2]rotaxane, l’anneau peut avoir un mouvement de translation le long de l’axe, ou bien un mouvement de rotation autour de l’axe.
Remarque : le chiffre [2] indique qu’il s’agit des structures les plus simples possibles : deux anneaux entrelacés, un anneau enfilé sur un axe.
Naissance de la topologie moléculaire
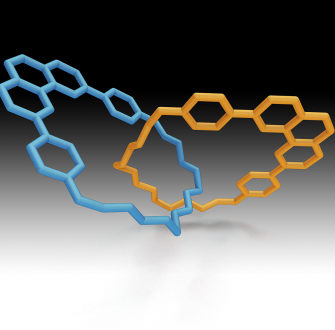
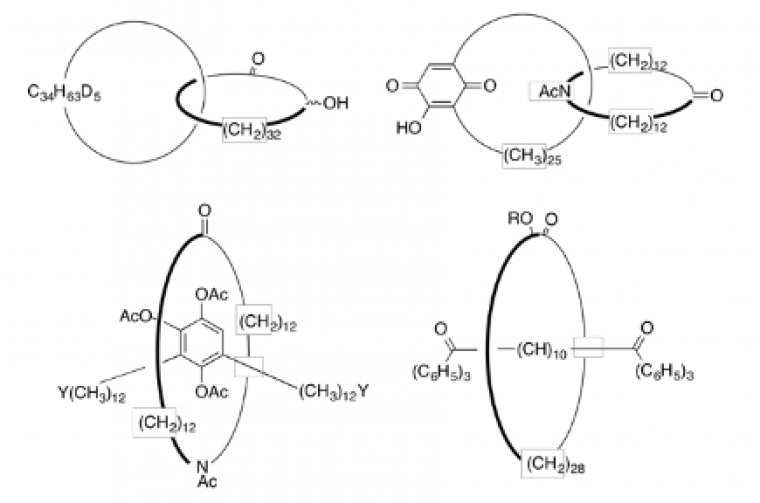
Les premières synthèses de molécules entrelacées datent des années 1960 ; elles conduisent à des assemblages de ce type :
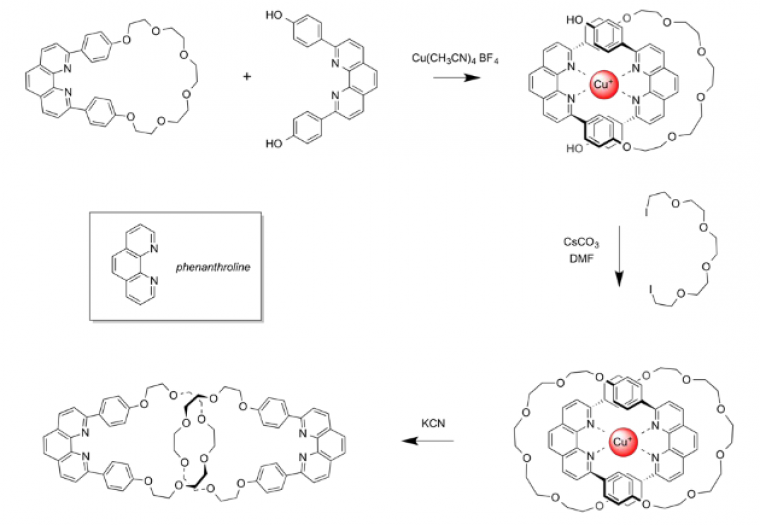
Les rendements sont faibles (quelques %). Les recherches se poursuivent dans les années 1970 mais c’est en 1983 qu’une avancée majeure a lieu. En effet, cette année-là, Jean-Pierre Sauvage et son équipe de recherche du CNRS, basée à l’Université de Strasbourg, mettent au point un procédé de synthèse utilisant la chimie organométallique et plus précisément la coordination entre un ion cuivre (I) et des entités phénanthroline, dont le rendement est bien meilleur (42 %).
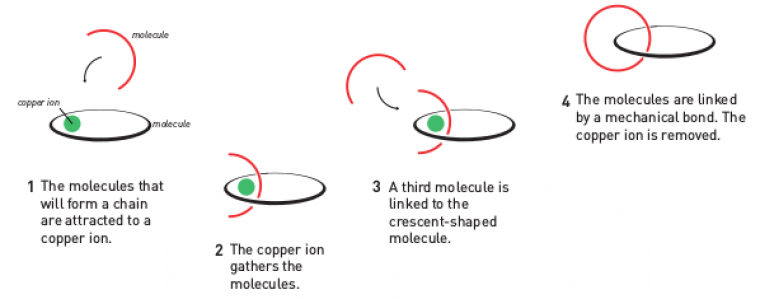
Le schéma de principe de la synthèse est le suivant :
Il y a d’abord coordination avec l’ion cuivre (I) d’une molécule en forme d’anneau (en noir ci-dessus) et d’une molécule en forme de croissant (en rouge ci-dessus). Ensuite, une troisième entité est liée de façon covalente à la molécule en forme de croissant et le deuxième anneau est créé. Enfin, une dernière réaction permet d’éliminer l’ion cuivre (I) et d’obtenir un assemblage de deux anneaux moléculaires, entrelacés l’un dans l’autre sans pour autant être lié de façon covalente.
Les réactions mises en jeu sont les suivantes :
Cette découverte marque le début de la topologie moléculaire, discipline qui consiste à imbriquer des molécules les unes dans les autres, sans liaisons covalentes entre elles. Jean-Pierre Sauvage continue dans cette voie, bientôt rejoint par James Fraser Stoddart (de l’université de Sheffield, au Royaume-Uni), et cherche à élaborer des structures de plus en plus complexes. Ainsi, un nœud de trèfle moléculaire (Jean-Pierre Sauvage), un anneau borroméen moléculaire (James Fraser Stoddart) ainsi qu’un nœud de Salomon moléculaire (Jean-Pierre Sauvage et James Fraser Stoddart) voient le jour (Figure 5).
Les premières machines moléculaires
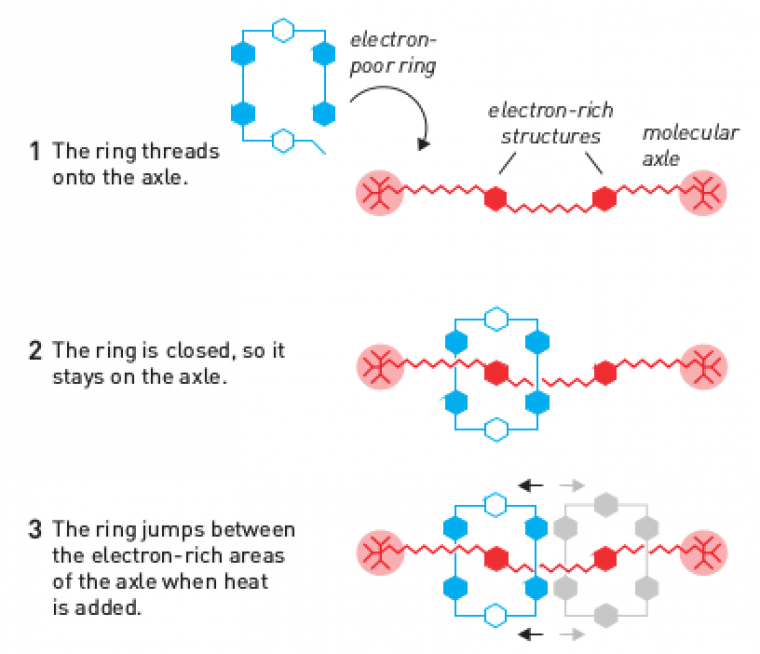
En 1991, Stoddart met au point un assemblage de type rotaxane, dans lequel l’anneau peut se déplacer le long de l’axe. Le principe est le suivant :
Au départ, l’anneau moléculaire (en bleu ci-dessus) est ouvert. C’est une structure pauvre en électrons, qui interagit favorablement avec les noyaux riches en électrons de l’axe moléculaire (en rouge ci-dessus). L’anneau est enfilé sur l’axe, puis fermé. L’axe comporte à ses extrémités des groupements volumineux qui empêchent l’anneau de s’échapper. L’anneau moléculaire peut adopter deux positions sur cet axe : celles correspondant aux deux cycles riches en électrons. On observe donc un mouvement de translation de l’anneau le long de l’axe (Figure 7).
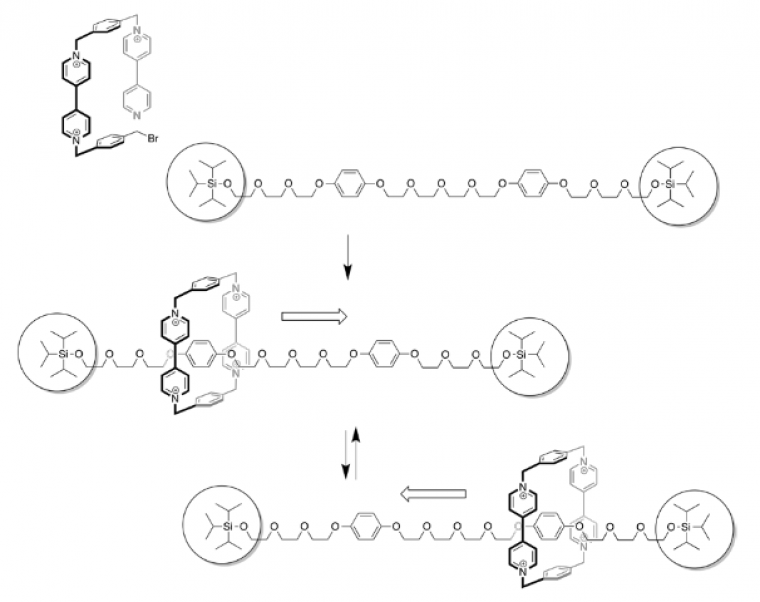
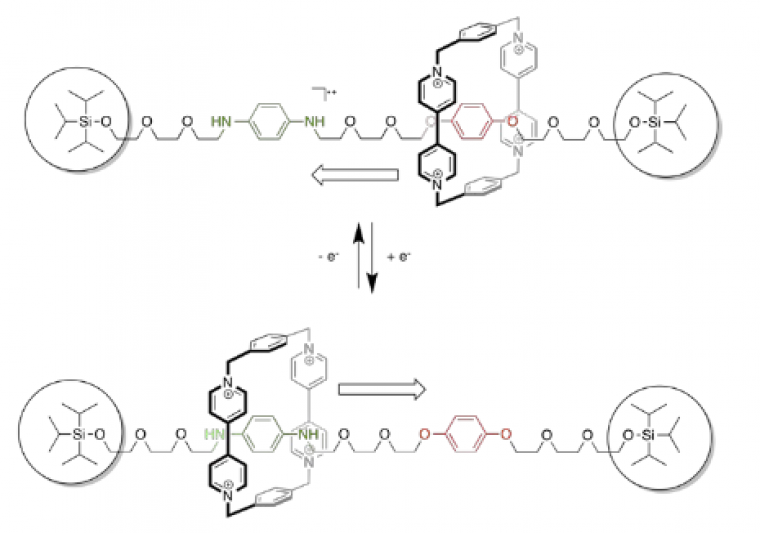
L’enjeu est alors de contrôler ce mouvement. En 1994, Stoddart y parvient, via un cycle d’oxydation/réduction : il utilise le même type de structure que précédemment à ceci près que les deux noyaux électrodonneurs de l’axe moléculaire sont différents :
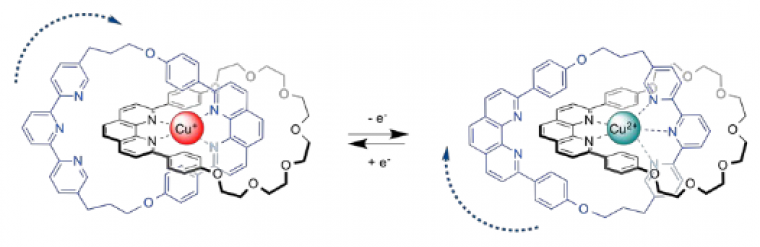
La même année, Jean-Pierre Sauvage met au point un dispositif dans lequel il peut contrôler un mouvement de rotation : il s’agit d’une structure de type caténane, dans laquelle l’un des anneaux comporte deux sites de coordination (phénanthroline et terpyridine) tandis que l’autre n’en comporte qu’un seul (phénanthroline) (Figure 9).
La rotation du premier anneau par rapport à l’autre peut être générée via l’oxydation ou la réduction de l’ion cuivre central.
Le contrôle de ces mouvements marque un tournant : les premières machines moléculaires sont nées !
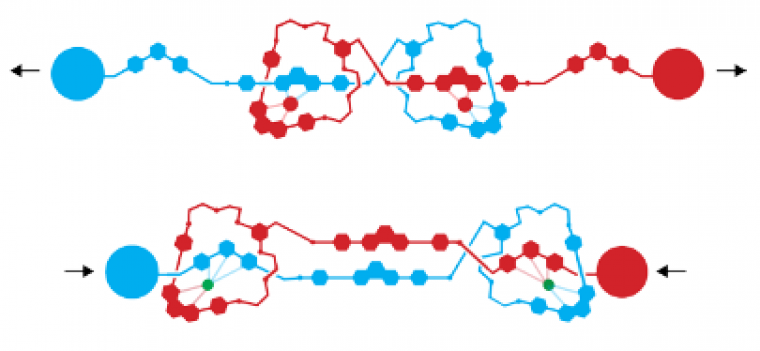
Durant la deuxième moitié des années 1990, les développements se poursuivent ; en 2000, Jean-Pierre Sauvage met au point un assemblage de deux rotaxanes entrelacés dans lequel il peut contrôler un mouvement de contraction/extension d’amplitude voisine de 2 nm. Il reproduit alors, à l’échelle moléculaire, le mouvement des fibres musculaires (Figure 10).
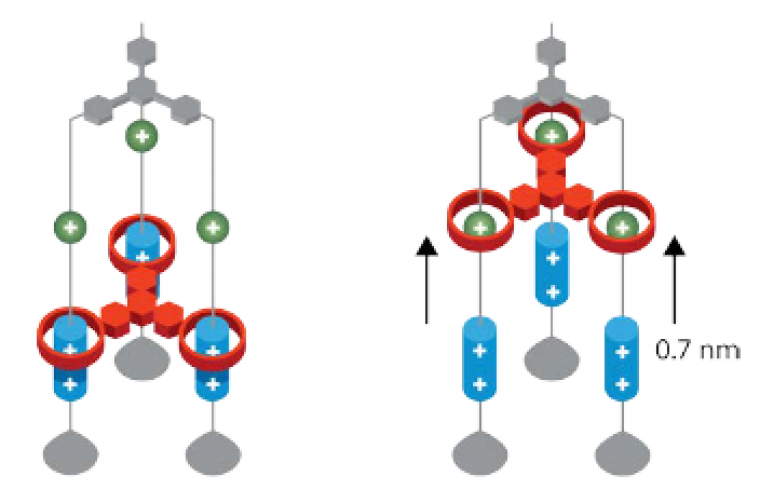
Dans le même temps, Stoddart met au point un dispositif qu’il appelle ascenseur moléculaire, dans lequel une entité peut se déplacer entre deux niveaux séparés de 0,7 nm (Figure 11).
Utiliser les liaisons multiples pour concevoir des moteurs moléculaires
Une autre approche consiste à contrôler le mouvement de rotation, toujours dans un même sens, d’une molécule sur elle-même, dans le but de concevoir un moteur moléculaire. Dans cette approche, les liaisons multiples (comme les doubles liaisons C=C) sont intéressantes, car la rotation autour de celles-ci est bloquée à température ambiante. Un apport d’énergie est nécessaire pour la provoquer, ce qui laisse entrevoir une possibilité de contrôler cette rotation, en contrôlant l’énergie à apporter.
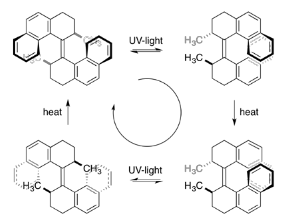
En 1999, les travaux de Bernard L. Feringa (de l'Université de Groningen, Pays-Bas) sur ce sujet aboutissent au premier dispositif moléculaire pouvant tourner sur lui-même, toujours dans le même sens, grâce à des cycles alternant irradiation UV et relaxation thermique. Le premier moteur moléculaire est né !
L’irradiation UV apporte l’énergie nécessaire à la rotation de 180° autour de la liaison double C=C centrale. Avec un apport d’énergie thermique, un cycle aromatique d’une partie de la molécule parvient à passer par-dessus celui d’une autre partie de la molécule : la rotation en sens inverse est alors bloquée. Une nouvelle irradiation UV génère une deuxième rotation à 180° autour de la double liaison C=C. Un deuxième apport d’énergie thermique permet aux groupes méthyles de passer sous les cycles aromatiques : le système retrouve sa position initiale. On observe que tout au long du mécanisme, la molécule tourne toujours dans le même sens (Figure 12). Bernard L. Feringa poursuit ses recherches et met au point, en 2014, un moteur moléculaire tournant à une fréquence de 12 MHz.
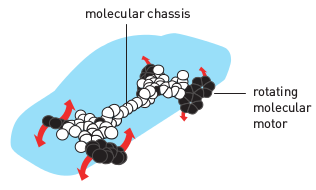
L’équipe de Bernard L. Feringa ne s’arrête pas là et se lance dans la construction d’une voiture moléculaire : un chassis maintient solidaires quatre de ces moteurs moléculaires jouant le rôle de « roues » qui, tournant toutes dans le même sens, permettent à cette « nano-voiture » d’avancer (Figure 13).
Conclusion
Les travaux pionniers de Jean-Pierre Sauvage, Sir James Fraser Stoddart et Bernard L. Feringa ont donné des outils aux chimistes du monde entier et ouvert la voie de la conception de machines moléculaires. En particulier, la construction de nano-voitures par l'équipe de Bernard L. Feringa a fait des émules et une course internationale de nano-voitures (Nano-Car Race), initialement prévue à l’automne 2016, devrait avoir lieu dans quelques mois.
Les Lauréats
Jean-Pierre SAUVAGE : de nationalité française, né en 1944 à Paris. Professeur émérite à l'Université de Strasbourg et directeur de recherche émérite au CNRS.
https://isis.unistra.fr/laboratory-of-inorganic-chemistry-jean-pierre-sauvage
Une vidéo de Jean-Pierre Sauvage présentant sa discipline est disponible sur le site du CNRS.
Sir James Fraser Stoddart : de nationalité écossaise, né en 1942 à Edimbourg, Ecosse. Board of Trustees Professor of Chemistry at Northwestern University, Evanston, IL, USA.
http://stoddart.northwestern.edu
Bernard L. Feringa : de nationalité hollandaise, né en 1951 à Barger-Compascuum, Pays-Bas. Professeur de Chimie Organique à l'Université de Groningen, aux Pays-Bas.
www.benferinga.com
Source : http://www.nobelprize.org