Les extractions sont parmi les méthodes les plus utilisées en analyse pour séparer les mélanges. Elles reposent sur la différence d'affinité d'un soluté entre deux phases non-miscibles entre elles. Nous donnons ici le principe de l'extraction liquide-liquide qui permet de transférer un soluté d'une phase liquide à une autre phase liquide non-miscible à la première.
Principe physico-chimique
L'extraction liquide-liquide repose sur la différence d'affinité d'un soluté entre deux phases liquides non-miscibles.
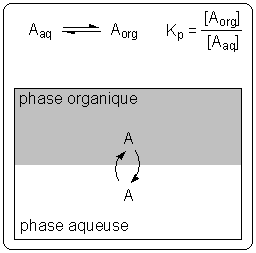
Considérons un soluté A en solution dans l'eau à extraire par une phase organique non-miscible à l'eau. Lorsque les deux phases liquides sont en contact il s'établit un équilibre de partage pour A (figure 1).
Cet équilibre est caractérisé par une constante thermodynamique $K_p$ appelée le coefficient de partage : $K_p=[A_{org}]/[A_{aq}]$1. L'extraction sera d'autant plus efficace que le coefficient de partage est grand; on choisit, lorsque cela est possible, un solvant d'extraction dans lequel le soluté est très soluble. Nous montrons au ci-après que les extractions multiples sont plus efficaces que l'extraction simple pour un même volume de solvant.
En pratique
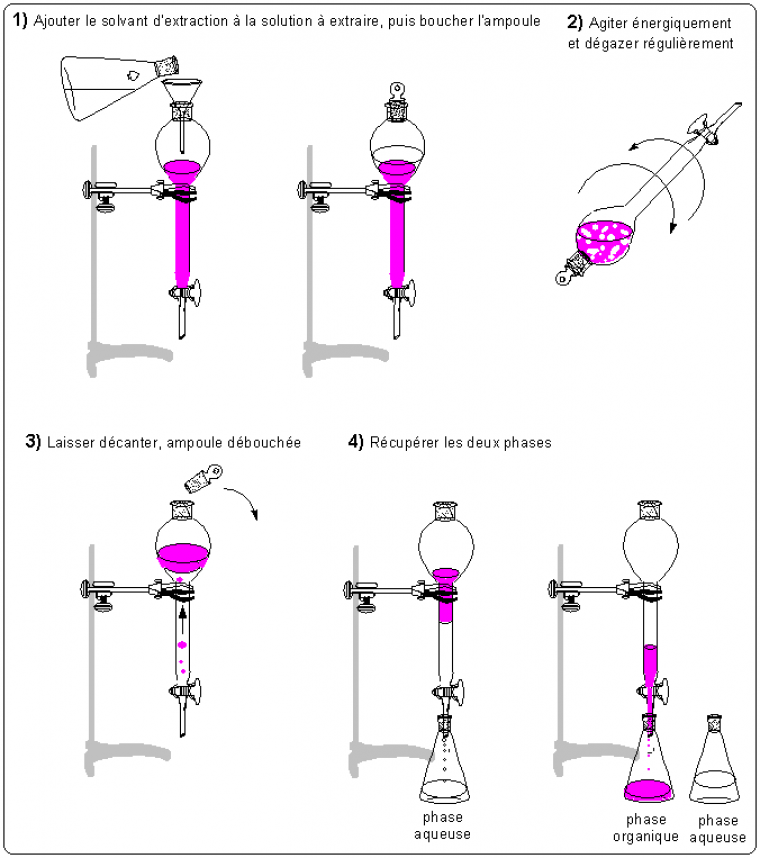
Au laboratoire de travaux pratiques, on travaille sur des volumes de solution à extraire de l'ordre de la centaine de mL au plus. On utilise pour cela des ampoules à décanter (figure 2). On choisit une ampoule de volume tel que les phases liquides occupent au maximum la moitié de l'ampoule. Par exemple pour extraire 30 mL de solution aqueuse par 10 mL d'éther, on utilise une ampoule de 100 mL plutôt qu'une ampoule de 50 mL.
Protocole d'extraction
- On introduit la solution à extraire et le solvant d'extraction dans l'ampoule à l'aide d'un entonnoir à liquide.
- Après avoir bouché l'ampoule, on la tient retournée, à deux mains, et on agite énergiquement. Pour extraire le soluté de façon optimale, il faut atteindre l'équilibre de partage précédent. Or si on laisse le contenu de l'ampoule sans agitation, l'interface entre les deux phases est très faible et la diffusion du soluté d'une phase vers l'autre est lente. L'agitation énergique de l'ampoule permet d'augmenter cette interface et d'atteindre l'équilibre plus rapidement.
Il faut prendre soin de dégazer entre chaque agitation pour éviter une surpression dans l'ampoule. En effet, l'équilibre de mélange peut être exothermique et entraîner une légère augmentation de température dans l'ampoule. Cela provoque une vaporisation du solvant le plus volatil qui met l'ampoule sous pression. Dans le cas de l'éther, très volatil, il peut être prudent de dégazer avant même la première agitation. - Il faut déboucher l'ampoule lorsqu'on la repose sur son support, toujours pour éviter une surpression. On doit ensuite laisser décanter les phases.
Il arrive parfois que des gouttes de la phase la moins dense adhèrent le long de la paroi de l'ampoule, au sein de la phase la plus dense. On peut les décrocher manuellement en introduisant une baguette de verre dans l'ampoule ou bien en la faisant tourner sur son axe en tenant le tube entre ses mains. - On récupère ensuite les deux phases séparément : la phase aqueuse est en générale plus dense que les phases organiques, à l'exception des solvants chlorés. Si on a un doute, on peut introduire une goutte d'eau dans l'ampoule et suivre son trajet.
On recommence l'extraction de la phase aqueuse avec une nouvelle fraction de phase organique. Une fois l'extraction terminée, on réunit toutes les phases organiques pour le séchage.
NB : Durant chacune de ces opérations, il est impératif de conserver toutes les phases (aqueuses et organiques) extraites, même si celles-ci ne vont plus nous servir, en cas d’erreur.
Exemple : l'extraction du diiode d'une solution aqueuse par le cyclohexane
Les différentes étapes mentionnées ci-dessus sont illustrées sur les photos ci-dessous. L'expérience est également filmée, voir la vidéo.
Optimiser les extractions : procéder par fractions
On peut montrer que pour un volume donné de solvant d'extraction, il est plus efficace de procéder en plusieurs extractions avec des fractions de ce volume qu'en une seule fois [1].
À titre d'exemple, considérons l'extraction de $n_0$ mole de A en solution dans aqueuse de volume $V_{aq}$ par un volume $V_{org}$ de solvant organique. La relation $K_p = [A_{org}]/[A_{aq}] = (n_{org}/V_{org}) / (n_{aq}/V_{aq})$ donne $n_{org} = (K_p V_{aq}/V_{org}) n_{aq}$.
Si on extrait une fois avec le volume $V_{org} = V_{aq}$, alors $n_{org} = K_p n_{aq}$ et comme $n_{org}+n_{aq}=n_0$, on obtient $n_{org} = 0,909 n_0$.
Si on extrait deux fois de suite avec $V_{org} = 0,5 V_{aq}$, alors $n_{org} = 0,5 K_p n_{aq}$ à chaque extraction.
-
première extraction : $n_{org} = 0,833 n_0$
-
deuxième extraction : $n_{org} = 0,833 (n_0 - 0,833 n_0) = 0,139 n_0$
Les phases organiques réunies contiennent $n_{org} = 0,972 n_0$, soit 6 % de plus de produit qu'en une seule extraction.
Réaliser les extractions difficiles
Transfert de phase
Le coefficient de partage $K_p$ est parfois inférieur à 1 ou seulement faiblement supérieur. C'est par exemple le cas pour les ions en solution aqueuse qui sont bien mieux solvatés par l'eau que par les solvants organiques. Dans ce cas $K_p$ est très inférieur à 1 et il est impossible d'inverser la tendance en changeant de solvant d'extraction. On peut quand-même extraire le soluté en utilisant un agent de transfert de phase.
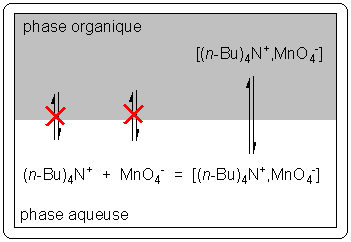
Un agent de transfert de phase est une substance qui réagit avec le soluté et le transforme en une espèce plus soluble dans le solvant d'extraction. Considérons par exemple les ions permanganate MnO4- en solution aqueuse à extraire par le toluène [2]. L'introduction de tétrabutylammonium (n-Bu)4N+ permet la formation de paires d'ions [(n-Bu)4N+, MnO4-], beaucoup plus solubles dans le toluène que les ions MnO4-. Cette augmentation de solubilité s'explique par la neutralité de l'édifice et la présence des chaînes butyle. Les équilibres mis en jeu dans cette procédure sont schématisés sur la figure 6.
Extraction en continu
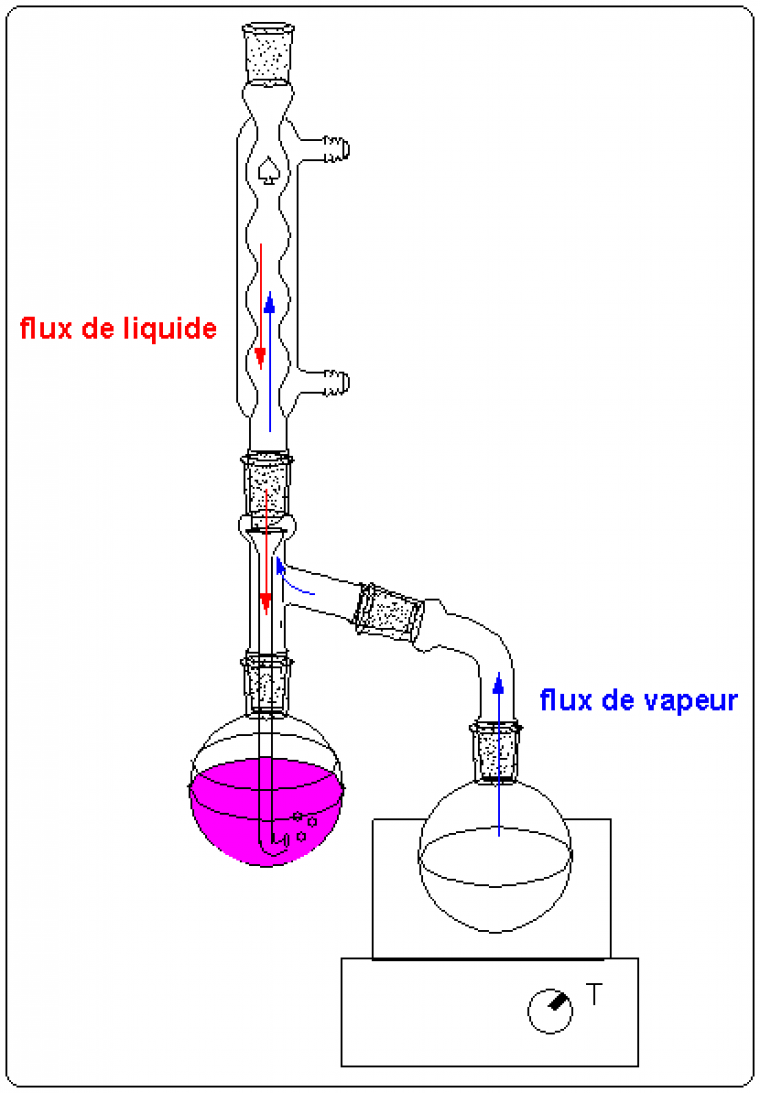
Si $K_p$ est très inférieur à 1 et que la nature du soluté ne permet pas de mettre en oeuvre le transfert de phase, on peut réaliser une extraction en continu. On utilise pour cela un montage qui permet de recycler le solvant d'extraction (figure 7).
Le montage de la figure 7 est utilisé lorsque le solvant d'extraction est moins dense que la solution à extraire. Les vapeurs de solvant d'extraction émises par le ballon se condensent sur le réfrigérant et le liquide ainsi formé traverse la solution à extraire de bas en haut en se chargeant de soluté au passage. Quand le niveau de liquide dans le ballon d'extraction est atteint le coude, le solvant d'extraction retourne dans le ballon d'ébullition où il est à nouveau vaporisé. Le ballon d'ébullition s'enrichit donc en soluté. Un dispositif analogue existe pour les solvants d'extraction plus denses que la solution à extraire [1,3].
Bibliographie et ressources en ligne
[1] D. Skoog, D. West, J. Holler, « Chimie analytique », 7ème éd. 1997. De Boeck Université.
[2] B. Fosset, C. Lefrou, A. Masson, C. Mingotaud, « Chimie physique expérimentale », 2000, Hermann.
[3] J.-P. Bayle, « 400 manipulations commentées de chimie organique volume 1 », 2006, Ellipses.
[4] J. Drouin, « Manipulations commentées de chimie organique », De Boeck Université, 1999, De Boeck.
[5] Animation sur l'extraction liquide-liquide sur le site du CEA