Il s'agit du premier article du dossier traitant de l'écocatalyse, domaine de la chimie verte associant phytoremédiation de régions polluées par des éléments métalliques et synthèse de molécules utilisant ces éléments métalliques comme catalyseurs. Les applications de l'écocatalyse sont nombreuses : domaines des colorants, des polymères, des cosmétiques et plus largement toute la chimie de synthèse.
Ce premier article (ci-dessous) aborde les notions de pollution métallique, de phytoremédiation et d'écocatalyse ; le deuxième article présente quelques exemples des performances de l'écocatalyse.
Introduction
Compte-tenu de leur immobilisme, les plantes se développent dans un milieu souvent hostile dont elles ne peuvent s’échapper. Elles subissent donc totalement les contraintes liées à leur environnement et doivent s’y adapter ou disparaître. Certaines plantes sont amenées à développer des mécanismes biologiques très particuliers pour répondre à des agressions telles que la sécheresse, l’attaque par les herbivores, les parasites, le piétinement, le stress oxydant et la pollution.
Quand on réalise que ces conditions varient continuellement, on ne peut qu'être fasciné par les stratégies mises en œuvre par les plantes pour survivre, se tenir, croître, être pollinisées, se disséminer, germer et résister face aux contextes changeants de leur environnement. La compréhension de ces processus est particulièrement importante dans un monde soumis à des changements globaux rapides. Ainsi, par exemple, certaines espèces végétales sont capables de se développer sur des terrains hautement contaminés en éléments métalliques, voire de séquestrer des polluants hautement toxiques dans leurs racines mais aussi dans leurs feuilles. Les plantes peuvent donc apporter des solutions originales à la décontamination des sols et des systèmes aquatiques.
Cette découverte est le point de départ d’un nouveau domaine de recherche, qui repose sur la combinaison inhabituelle des domaines de l’environnement, de l’écologie et de la chimie verte.
Il s’agit, pour la première fois, d’associer réhabilitation écologique de milieux dégradés et/ou pollués par les Éléments Traces Métalliques (ETM) et procédé innovant de valorisation chimique des phytotechnologies associées.
La pollution métallique : une menace pour les sols et l’eau
Les activités anthropiques, domestiques, agricoles et industrielles, sont à l’origine d’une pollution des sols et des systèmes aquatiques par dispersion des ETM. Il s’agit d’un problème très préoccupant car le sol exerce des fonctions essentielles qui déterminent en grande partie la production des produits alimentaires et la qualité de l’eau. De plus, les ETM font partie des composés les plus nocifs. Ils ne sont pas biodégradables, mais persistants dans les organismes et les écosystèmes contaminés. Si certains ETM sont utiles à l’organisme (Zn, Fe, Mg, Cu, Ni, Co, Mo, Mn) comme cofacteurs d’enzyme, biocatalyseurs ou constituants de molécules essentielles à la vie (Mg dans la chlorophylle, Fe dans l’hémoglobine), ils deviennent toxiques à partir d’un certain seuil. D’autres ne présentent aucune activité biologique et sont toxiques en très faible quantité (Cd, Pb, Cr, Hg, Sn, As). Les conséquences de la dispersion des ETM dans l’environnement sont clairement établies :
- les pollutions métalliques conduisent à une érosion des sols, voire une phytotoxicité des systèmes sols ;
- l’érosion des sols entraîne une migration des ETM dans les systèmes sols-eau et une contamination des rivières ;
- ces phénomènes réduisent la fertilité des sols et entraînent la contamination des produits agricoles et alimentaires.
Ces scénarios constituent également une véritable menace pour l'accès aux ressources en eau potable. Du fait de leurs propriétés physiques intéressantes (conduction électrique et thermique, dureté, malléabilité, possibilités d’alliages, propriétés catalytiques, etc.) les métaux sont très largement utilisés. Les gisements métallifères sont exploités depuis longtemps. L’activité minière est à l’origine d’une dispersion des métaux dans l’environnement. Le milieu aquatique est alors contaminé par les eaux de ruissellement. Malgré le durcissement des réglementations, l’industrie est toujours responsable de la majorité des rejets directs dans l’eau. Par ailleurs, le traitement des minerais et l’industrie métallurgique restent à l’origine d’émissions importantes. Les activités agricoles sont également à l’origine d’une contamination de l’environnement. Par exemple, le sulfate de cuivre (bouillie bordelaise) est toujours utilisé pour traiter les vignes et les arbres fruitiers. Les engrais, les fongicides, les boues des stations d’épuration, les composts ou le lisier utilisés pour amender les surfaces agricoles sont également susceptibles d’être contaminés par les métaux. Le problème est largement amplifié dans les pays en développement.
Les effets cumulés de l’évolution climatique (sécheresses, pluies intenses mais courtes, réchauffement global) et les différentes formes de pollutions évoquées, associées à une surconsommation de l’eau et des produits agro-alimentaires font craindre à court terme une raréfaction des ressources vitales.
Préserver la qualité de l’eau, des sols et de l’air est ainsi devenue une priorité. Il y a donc une réelle nécessité à développer des technologies inventives et efficaces de restauration des sites, zones et écosystèmes pollués.
La phytoremédiation : une solution naturelle
Aujourd’hui, la prise de conscience de la portée de ces problèmes environnementaux transforme le concept de la phytoremédiation en pistes d’actions concrètes. La présence et l’étude des organismes adaptés à une situation de pollution industrielle permettent de définir de nouvelles approches de remédiation intégrées et bio-inspirées. Elles s’inscrivent dans le cadre d’une écologie globale, qui mobilise différents champs disciplinaires de l’écologie scientifique (végétale, microbienne, moléculaire, évolutive, fonctionnelle, chimique), de la biologie, de la toxicologie, de la physico-chimie et de la chimie du vivant. Deux scénarios sont envisageables : la stabilisation ou la remédiation active des sites dégradés. Ces techniques de remédiation peuvent être schématiquement réparties en deux grands secteurs :
- la bioremédiation ;
- la phytoremédiation.
La bioremédiation repose sur l’utilisation d’espèces bactériennes spécifiques et adaptées à la décontamination de zones contaminées, notamment par les polluants organiques ou les radionucléides.
ETM désigne l'élément trace métallique
La phytoremédiation est plutôt destinée à la résolution de problèmes environnementaux générés par les ETM. Compte tenu de leur phytotoxicité, les sols métallifères exercent une forte pression de sélection et génèrent des habitats particuliers pour les espèces végétales et les micro-organismes associés. Il en résulte une ressource biologique unique, les métallophytes [1]. Ces métallophytes sont définis comme étant capables de tolérer des concentrations élevées en ETM, de survivre et de se reproduire sur de tels sites [2].
Les procédés de phytoremédiation les plus connus sont :
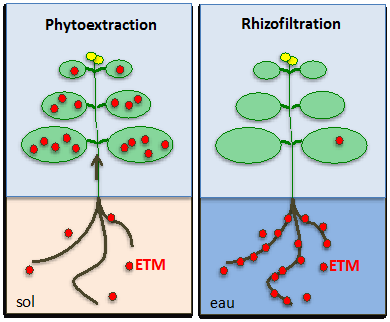
- la phytoextraction : les polluants sont extraits par les plantes et stockés dans leurs tissus (feuilles ou racines) : les plantes utilisées sont dites hyperaccumulatrices ;
- la phytostabilisation : elle consiste à recouvrir les sols par des espèces végétales capables d’immobiliser la pollution ;
- la rhizofiltration : le procédé de phytostabilisation s’effectue en milieu aquatique au niveau de la rhizosphère.
La phytoextraction et la rhizofiltration constituent deux technologies naturelles de dépollution des sols, pour la première, et de l’eau, pour la seconde.
Cependant, le développement de ces deux phytotechnologies de dépollution naturelle est resté limité par absence de valorisation de la biomasse contaminée. Sans débouché crédible, les parties aériennes des plantes hyperaccumulatrices ou les racines des espèces utilisées en rhizofiltration, sont considérées comme des déchets contaminés. L’essor de la phytoextraction et de la rhizofiltration est entièrement lié à la valorisation de la biomasse générée.
L’écocatalyse : une valorisation inédite de la phytoextraction et de la rhizofiltration
Les deux stratégies les plus signifivatives de recyclage des plantes hyperaccumulatrices d’ETM reposent sur deux filières classiques et indépendantes :
- la filière inspirée du traitement de la biomasse : bioénergie et plus particulièrement la filière bois-énergie [3-5] ;
- la filière inspirée du traitement du minerai : l’hydrométallurgie adaptée aux métaux d’origine végétale ou phytoextraction minière (phytomining [6,7]).
Dans le cas de la filière bois-énergie, deux problèmes immédiats encore non résolus concernent le devenir des résidus de combustion (et de leur toxicité éventuelle) des plantes hyperaccumulatrices, ainsi que la volatilité des espèces métalliques lors de la combustion, qui posent des problèmes immédiats de sécurité environnementale [3-5]. Beaucoup de questions restent donc en suspens.
Dans le cas de la phytoextraction minière, le procédé nécessite la séparation des éléments métalliques, la réduction de l’élément phytoextrait au degré zéro et la production massive de biomasse pour atteindre des quantités exploitables de métal. Le coût global du procédé est donc nivelé par les traitements délicats et coûteux de la biomasse qui sont inhérents à l’application ciblée (formation de métal pur au degré d’oxydation zéro à l’aide de sels de nickel dont les particules doivent être de taille et de morphologie précises). La rentabilité du procédé reste donc vulnérable et très exposée aux fluctuations du cours du métal ciblé.
Le laboratoire de chimie bio-inspirée et d’innovations écologiques (UMR 5021 Chim-Eco CNRS-Université de Montpellier) a proposé une valorisation inédite de la phytoextraction et de la rhizofiltration, l’écocatalyse. Les déchets végétaux générés sont valorisés à travers un concept innovant de recyclage écologique. Tirant parti de la capacité remarquable de certains végétaux à bioconcentrer des ETM, l’écocatalyse repose sur l’utilisation inédite des espèces métalliques d’origine végétale comme réactifs et catalyseurs de réactions de chimie organique fine. Elle permet la préparation de biomolécules selon une approche éco-responsable et bio-inspirée [8-9].
Grâce à l’écocatalyse, la biomasse issue de la phytoextraction et de la rhizofiltration n’est plus un déchet contaminé mais un système naturel de restauration qui possède une haute valeur ajoutée. Cette biomasse constitue un réservoir naturel de métaux de transition précieux en synthèse organique. En d’autres termes, des déchets indésirables sont devenus des objets chimiques utiles, innovants et motivants.
L’écocatalyse : une catalyse chimique bio-sourcée
Les objectifs de valorisation de la phytoextraction par écocatalyse se démarquent clairement des rares essais de valorisation précédemment décrits dans la littérature.
Le procédé de chimie verte proposé repose sur des bases chimiques particulièrement adaptées aux nouvelles orientations de l’industrie chimique, celles de la catalyse métallique. Cette démarche est inédite. La catalyse en chimie organique est un exemple démonstratif de chimie durable en ce sens où elle peut devenir le moteur d’une industrie chimique nouvelle. Peu consommatrice en matière première métallique, elle est adaptée au procédé de valorisation par catalyse, car elle ne nécessite pas de gros rendements de phytoextraction ; 0,1 à 2 % en espèces métalliques MXn sont généralement suffisants pour catalyser une réaction de synthèse ; si le catalyseur est supporté sur un solide, les espèces métalliques deviennent recyclables et utilisables en continu.
En outre, la nature chimique de l’espèce métallique phytoextraite correspond au degré d’oxydation directement utilisable en synthèse organique. Aucune phase de réduction du cation métallique n’est nécessaire. Le procédé est nécessairement sobre et peu onéreux.
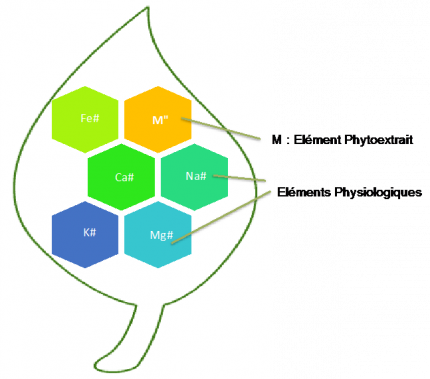
L’écocatalyse permet le recyclage de ressources minérales très variées telles que Zn2+, Ni2+, Mn2+, Cu2+, Co2+, Pd2+ par les plantes métallophytes. Les feuilles ou les racines des plantes gorgées de métaux sont traités thermiquement afin d’éliminer une partie de la matière organique et de concentrer la partie minérale. La poudre minérale obtenue est ensuite activée pour augmenter son activité catalytique. L’écocatalyseur brut possède une structure polymétallique, résultant de la combinaison du métal phyto-extrait (par exemple Zn2+, Ni2+, Mn2+, Cu2+ ou Pd2+) avec des cations physiologiques, c’est-à-dire avec des éléments classiques généralement nécessaires au développement des plantes (par exemple Na+, K+, Ca2+, Mg2+, Fe3+). La composition et la structure de cet écocatalyseur brut sont complexes et originales. Elles reflètent la physiologie de la plante dont elles sont issues ; on parle d’empreinte végétale.
Les extraits multi-métalliques obtenus offrent une opportunité unique d’exploitation de la catalyse coopérative dans laquelle la synergie et la sélectivité sont prometteuses. En effet, la présence simultanée d’une combinaison de sites actifs bien définis résulte de cette variété d’espèces métalliques. Dès lors, des séquences d’étapes réactionnelles originales permettent d’aboutir à des sélectivités uniques. Un catalyseur classique pourrait en effet se limiter à influencer seulement certaines des étapes du processus réactionnel, limitant ainsi les opportunités en synthèse organique. Ici, la richesse des différentes interactions entre les espèces présentes conduit à des interactions métal/ligand inhabituelles en solution.
En biologie, on désigne par « coopérativité » une propriété des protéines, des enzymes ou de récepteurs qui possèdent au moins deux sites de fixation de substrats ou de ligands. Une protéine est qualifiée de coopérative si les fixations des différents substrats/ligands ne sont pas indépendantes mais se renforcent mutuellement : la fixation d’un premier substrat/ligand sur un site augmente l’affinité d’un autre substrat/ligand pour un autre site. La coopérativité est utile et productive, même en chimie…
Les écocatalyseurs peuvent servir de catalyseurs hétérogènes ou homogènes dans des transformations synthétiques permettant l’accès à des molécules ayant une haute valeur ajoutée pour la chimie fine et industrielle (arômes et cosmétiques ayant le label « naturel », médicaments, oligomères d’intérêt biologique, hétérocycles aromatiques fonctionnalisés, agents bio-répulsifs d’insectes nuisibles, intermédiaires-clés de procédés chimiques industriels variés et matériaux organiques).
Bibliographie et références (communes aux deux articles du dossier)
- Baker A.J., Ernst W.H., Van der Ent A. et al., « Metallophytes : the unique biological resource, its ecology and conservational status in Europe, Central Africa and Latin America », Ecology of Industrial Pollution, Cambridge University Press, Cambridge 2010, 7-40.
- Van der Ent A., Baker A.J.M., Reeves R.D. et al., « Hyperaccumulators of metal and metalloid trace elements : facts and fiction », Plant Soil, 2013 362, 319-334.
- Bert V., Seuntjens P.Dejonghe W.Lacherez S.Thi Thanh Thuy H.Vandecasteele B. Phytoremediation as a management option for contaminated sediments in tidal marshes, flood control areas and dredged sediment landfill sites. Environmental Science and Pollution Research 2009, 16, 745 – 764
- Bert V, Tack K, Vialletelle F, Magnie MCL, Berquet A, Cochet N, Schoefs O. Prospects in biomass valorization from phytoextraction of Cd, Pb and Zn with hyperaccumulators. Recents Progrès en Génie des Procédés, 2009, 98: 297-1:6, Ed. SFGP, Paris (Fr).
- Delplanque M., Collet S., Del Gratta F. et al., « Combustion of Salix used for phytoextraction : the fate of metals and viability of the processes », Biomass & Bioenergy, 2013, 49, 160-170.
- Chaney, R.L., Angle, J.S., Baker, A.J.M., Li, Y.M.. Method for phytomining of nickel, cobalt and other metals from soils. U.S. Patent 5 711 784 1998.
- Bani, A (2009), Thèse de l’Université Agricole de Tirana
- Grison C., Special Issue in Environmental Science and Pollution Research (Ed. Invite C. Grison) : Combining Phytoextraction and EcoCatalysis: an Environmental, Ecological, Ethic and Economic Opportunity, Environ. Sci. Pollut. Res. 2015,22, 5589-5698.
- P.-A. Deyris, C. Grison, Nature, Ecology and Chemistry : an unsual combination for a new green catalysis, Ecocatalysis, Curr. Opin. Green Sustain. Chem. 2018 (Ed. invited) doi :10.1016/ j.cogsc.2018.02.002.
- Grison C.M., Escande V., Petit E., Garoux L., Boulanger C., Grison C. Psychotria douarrei and Geissois pruinosa, novel resources for the plant-based catalytic chemistry, RCS Advances, 2013, 3(44), 22340-22345.
- Thillier Y., Losfeld G., Escande V., Dupouy C., Vasseur J-J., Debart, F. Grison C., Solid-phase synthesis of 5’-capped RNA with polymetallic catalysts prepared from metallophytes species, RCS Advances 2013, 3 (15), 5204-5212.
- P.-A. Deyris, E. Petit, Y.-M. Legrand, S. Diliberto, C. Boulanger, V.Bert, C. Grison, Biosourced polymetallic catalysis : A surprising and efficient means to promote the Knoevenagel condensation, Front. Chem.2018. doi : 10.3389/fchem.2018.00048, P.-A. Deyris, E. Petit, Y.-M. Legrand, S. Diliberto, C. Boulanger, V.Bert, C. Grison
- V. Escande, C. Poullain, G. Clavé, E.Petit, N. Masquelez, P. Hesemann, C. Grison, Alternative Green and Ecological Input for Transfer Hydrogenation using EcoNi(0) Catalyst in Isopropanol, Applied Catalysis B., 2017, 2017, 210, 495-503.
- V. Escande, C. H. Lam, C. Grison, P.T. Anastas, EcoMnOx, a Biosourced Catalyst for Selective Aerobic Oxidative Cleavage of Activated 1,2-Diols, ACS Sustainable Chem. Eng., 2017, 5 (4), pp 3214–3222
- Escande V., Petit E., Garoux L., Boulanger C., Grison C., Switchable alkene epoxidation/oxidative cleavage with H2O2-NaHCO3: efficient heterogeneous catalysis derived from biosourced Eco-Mn, ACS Sustainable Chem. Eng., 2015, 3 (11), 2704–2715.
- Escande V., Garoux L., Grison C.M., Thillier Y., Debart F., Vasseur J.J., Boulanger C., Grison C., Ecological catalysis and phytoextraction Symbiosis for future, Appl. Catal. B, 2014, 146, 279-288.
- Escande V., T.K. Olszewski, E. Petit, C. Grison Biosourced Polymetallic Catalysts : An Efficient Means To Synthesize Underexploited Platform Molecules from Carbohydrates, ChemSusChem, 2014, 7, 1915-1923. .
- Escande V., Velati A., Garel C., Renard B.L., Petit, E., Grison C., Phytoextracted mining wastes for Ecocatalysis : Eco-Mn®, an efficient and eco-friendly plant-based catalyst for reductive amination of ketones, Green Chemistry, 2015, 17, 2188-2199.
- Losfeld G., Vidal de la Blache P., V. Escande V., L’huillier L., Jaffre T., Grison C. The chemical exploitation of nickel phytoextraction : an environmental, ecologic and economic opportunity for New-Caledonia, Chemosphere, 2012, 89 (7) 907-910.
- G. Clavé, F. Pellissier, S. Campidelli, C. Grison Ecocatalyzed Suzuki-Miyaura cross coupling of heteroaryl compounds, Green Chem. 2017,19, 4093-4103
- G. Clavé, L. Garoux, C. Boulanger, P. Hesemann. C. Grison, Ecological Recycling of a Bio-Based Catalyst for Cu Click Reaction : a New Strategy for a Greener Sustainable Catalysis, Chemistry Select, 2016, 1410-1416
- Clavé G., Garel C., Poullain C., Renard B.L., Lange B., Shutcha M., Faucon M.P., Grison C., Ulmann reaction through ecocatalysis: insights from bioressource and synthetic potential, RCS Advances 2016, 6, 59550–59564.