La conception de nanoparticules pour la délivrance de molécules thérapeutiques vers un organe, un tissu ou une cellule malade, représente un enjeu majeur dans le domaine de la nanomédecine. Dans ce contexte, les chercheurs de l’Institut Galien Paris-Sud à Châtenay-Malabry (CNRS / Université Paris-Sud) ont développé une nouvelle famille de nanoparticules biocompatibles à forte activité anticancéreuse. Ils sont parvenus à faire croître, de manière contrôlée et ajustable, de courtes chaînes de polyisoprène à partir de molécules anticancéreuses, pour former des composés qui s’auto-assemblent sous forme de nanoparticules biologiquement actives in vivo. Ces résultats sont publiés dans la revue Angewandte Chemie.
Nanotechnologie et nanomédecine
La nanomédecine, qui représente l’utilisation des nanotechnologies dans le domaine biomédical, connaît actuellement un essor formidable. Elle a notamment conduit à de nombreuses avancées technologiques dans la conception de nano-assemblages organiques ou inorganiques (de diamètres allant de quelques dizaines à quelques centaines de nanomètres) capables de transporter des molécules thérapeutiques vers un organe, un tissu ou une cellule malade. La stratégie la plus employée à l’heure actuelle est l’encapsulation de principes actifs au sein de systèmes nanoparticulaires (liposomes, micelles, nanoparticules, etc).
Néanmoins, même si cette approche a conduit à de nombreux résultats très prometteurs, particulièrement en oncologie, certains verrous technologiques d’envergure demeurent : taux de chargement en principe actif souvent très faibles (quelques pourcents) et possible fuite du nano-transporteur bien avant que ce dernier ait atteint son site d’action. Ces deux paramètres peuvent conduire à des effets toxiques rédhibitoires.
A la recherche d'un système biocompatible innovant
C’est dans cette optique que des chercheurs de l’équipe du Prof. P. Couvreur à l’institut Galien Paris-Sud à Châtenay-Malabry ont conçu un nouveau système nanoparticulaire biocompatible à base de caoutchouc naturel synthétique, à la fois simple et innovant, où chaque molécule anticancéreuse est liée de manière covalente à une courte chaîne de polyisoprène1.
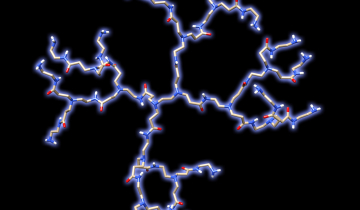
Ces prodrogues1 macromoléculaires, qui s’auto-assemblent sous la forme de nanoparticules biologiquement actives in vivo, possèdent des taux de chargement en molécules actives très nettement augmentés (plusieurs dizaines de pourcents). De plus, la libération de ces dernières est maintenant régie par hydrolyse ce qui empêche leur fuite précoce des nanoparticules. La construction de ces nanoparticules est elle aussi novatrice (cf. figure).
L’anticancéreux est modifié chimiquement pour servir d’amorceur lors de la polymérisation contrôlée (procédé permettant de bien contrôler l’ensemble des caractéristiques macromoléculaires du polymère) de l’isoprène. Ainsi, la longueur de chaîne du polyisoprène peut être aisément ajustée afin de conduire aux nanoparticules les plus efficaces. Cette découverte pourrait être appliquée à de nombreux autres principes actifs, ce qui permettrait à la mise au point de nouvelles nanoparticules biologiquement actives contre d’autres pathologies.
Références et ressources en ligne
[1] Harrisson, S. ; Nicolas, J. ;* Maksimenko, A. ; Bui, D. T. ; Mougin, J. ; Couvreur, P. ; Nanoparticles with In Vivo Anticancer Activity from Polymer Prodrug Amphiphiles Prepared by Living Radical Polymerization ; Angew. Chem., Int. Ed 17 décembre 2012, DOI : 10.1002/anie.201207297.