Cet article fait partie du dossier présentant le développement chimique, branche de l'industrie pharmaceutique qui participe au développement de la synthèse des principes actifs des médicaments et produit les lots nécessaires aux études cliniques avant commercialisation.
Le premier article rappelle les différentes phases de la « vie » d'un médicament, de la découverte du principe actif à la commercialisation.
Le deuxième article décrit les missions des équipes travaillant au développement chimique.
Le troisième article (ci-dessous) traite du scale-up, autrement dit la transposition à grande échelle d'une synthèse élaborée en laboratoire.
Un glossaire, commun aux trois volets, est accessible à la fin de chaque volet.
Venons-en maintenant à un aspect du quotidien des plus intéressants, le scale-up. C’est lui qui fait toute l’importance de notre métier et qui souvent met à mal les chimistes. Vous êtes-vous déjà fait peur en voyant votre ballon brûler ou exploser sous votre hotte ? Vous est-il déjà arrivé d’être incapable de reproduire une réaction sur quelques grammes alors qu’elle marchait parfaitement sur quelques milligrammes ? Imaginez maintenant les conséquences sur des mètres cubes de milieu réactionnel…
Attention au scale-up - Notre quotidien
Le scale-up fait partie intégrante de notre travail et il est généralement la source de nombreuses problématiques. Le critère le plus important du scale-up est la sécurité : si une synthèse ne peut pas être transposée à grande échelle avec sécurité, alors elle ne doit pas être transposée du tout !
La sécurité au cœur de notre attention
La notion de sécurité met en jeu deux principaux aspects :
- le transfert thermique et la réactivité (libération de chaleur, de gaz, etc.) ;
- le danger lié à la toxicité (pour l’homme, pour l’environnement, etc.). Un produit toxique peut être manipulé en toute sécurité avec les outils adéquats, mais un produit très réactif doit être maîtrisé, sans quoi les conséquences peuvent être désastreuses.
Des catastrophes sanitaires et écologiques se sont déjà produites et illustrent l’importance de la sécurité, comme les explosions de Flixborough en 1974, de Seveso en 1976, ou de Toulouse en 2001.
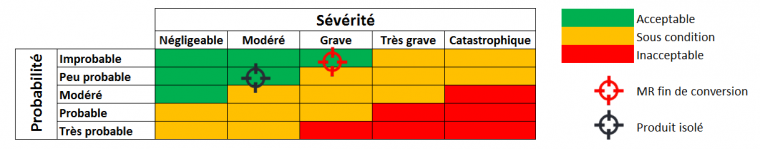
Toutes les réactions transposées à l’échelle semi-industrielle ou industrielle doivent faire l’objet d’analyses de risques. Une réunion se tient alors entre les chimistes et les personnes en charge de la sécurité des procédés pour se poser les bonnes questions : « Que se passerait-il si… ? » … si le système de refroidissement venait à s’arrêter, si le condenseur venait à tomber en panne, si tout le réactif était ajouté trop rapidement ? Toutes les phases de la synthèse sont ainsi analysées : la préparation du matériel, le chargement, la réaction chimique, le traitement des déchets, le stockage, pour faire en sorte que la probabilité d’un accident soit proche de zéro. Les réactifs et les produits sont analysés thermiquement à l’aide de la calorimétrie différentielle à balayage (Differential Scanning Calorimetry, DSC) qui permet de mesurer leur potentiel énergétique comparé à une référence inerte. La réaction est finalement classée dans un diagramme de risque représentant la sévérité en fonction de la probabilité d’un accident (voir Figure 1 ci-dessous).
Une décision est alors prise conjointement avec les personnes de la sécurité pour poursuivre ou non la montée en échelle de la synthèse (Go/no Go). Si la réaction ou les produits formés lors de celle-ci sont jugés inacceptables en termes de sécurité, la synthèse doit alors être remaniée.
Un transfert thermique difficile à extrapoler
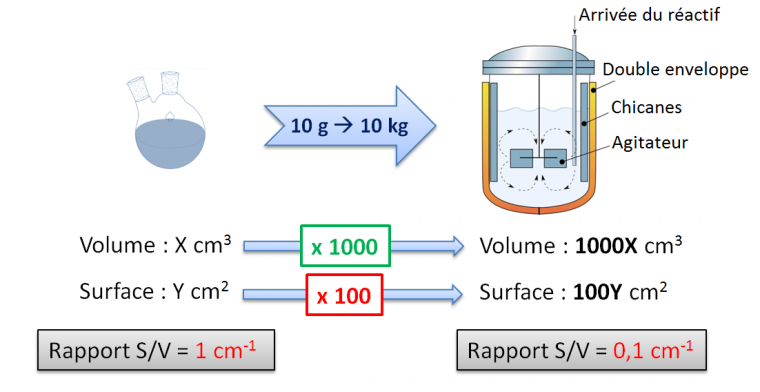
L’une des difficultés rencontrées durant le scale-up est liée aux transferts de chaleur. Une montée en échelle en chimie signifie automatiquement l’utilisation d’un matériel adéquat sur de plus grosses capacités. L’augmentation des dimensions joue en notre défaveur : une question insignifiante lorsque nous nous penchions sur notre ballon rempli de quelques milligrammes de produit durant nos études devient critique sur des grandes quantités. Ce point est illustré simplement ci-dessous.
Le volume est une fonction cubique du rayon de la sphère alors que sa surface est une fonction quadratique du même rayon. Une montée en échelle implique forcément une diminution du rapport surface/volume (S/V). Concrètement, plus le scale-up est important, plus il est difficile d’extrapoler la régulation de température d’un milieu réactionnel car la surface du réacteur n’évolue pas aussi vite que son volume. D’un point de vue sécurité, plus on monte en échelle, moins on a de surface d’échange pour refroidir un milieu réactionnel dont la température s’élève, du fait de l’exothermicité d’une réaction par exemple, d’où les risques d’emballement et d’explosion. Par ailleurs, le temps de chauffe peut augmenter, engendrant des problèmes de stabilité thermique des réactifs.
Il faut donc garder en mémoire que les transferts de chaleur au laboratoire sont complètement surdimensionnés par rapport à ceux de l’échelle industrielle. Tout ceci est donc à évaluer en amont et une question résonne dans la tête du jeune chercheur en chimie des procédés : Comment s’adapter à ces contraintes physiques ?
Des parades existent pour pouvoir réaliser nos réactions en toute sécurité : l’une d’entre elles est de conduire une réaction en semi-batch. Le principe d’un semi-batch est d’ajouter un réactif au fur et à mesure de sa consommation dans la réaction. Cela nous permet de contrôler de nombreux paramètres :
- la quantité de chaleur libérée par la réaction : le seul fait d’arrêter la coulée arrête le dégagement de chaleur et les problèmes de surface d’échange pour le refroidissement disparaissent.
- l’accumulation ce phénomène apparaît lorsqu’un réactif est ajouté plus vite qu’il ne réagit. L’accumulation de réactif pour une réaction exothermique conduit à une accumulation d’énergie et à une élévation de température potentiellement non maîtrisable, engendrant un risque d’explosion. Cela implique qu’il faut connaître la cinétique de réaction pour déterminer la vitesse d’addition optimale.
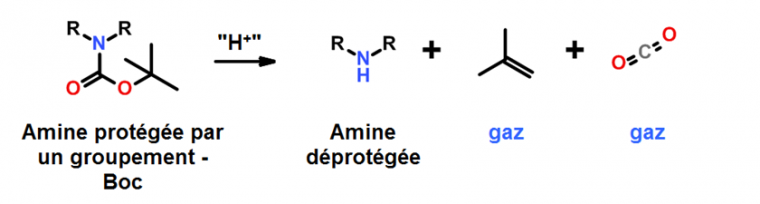
- le dégagement gazeux : prenons l’exemple d’une réaction de déprotection d’un groupement –Boc, qui libère deux moles de gaz par mole de réactif (Figure 3).
Imaginons 10 kg de réactif dans un réacteur, le fait d’ajouter tout l’acide d’un coup libèrerait une quantité énorme de gaz, faisant exploser immédiatement le réacteur. Ajouter le réactif en semi-batch sur l’acide permet de contrôler l’évolution de gaz.
- les réactions parasites : imaginons la suite de réactions suivantes :
A + B → C
B + C → impuretés
Ajouter B en semi-batch diminue logiquement les risques de former des impuretés.
Une autre possibilité est d’augmenter la surface d’échange thermique d’un réacteur : pour cela, l’idée est d’étirer le réacteur vers le haut pour l’amincir. En extrapolant ce procédé jusqu’à obtenir un tube, on crée la chimie en flux continu (pour plus d’informations : J. Org. Chem. 2013, 78, 6384).
On n’agite pas, on mélange !
Le transfert chimique de matière est également un aspect important à prendre en compte pour une montée en échelle réussie. Que cherche-t-on à faire lorsque l’on met en marche l’agitation d’un réacteur ? On sait qu’ « augmenter la probabilité de rencontre de deux molécules de réactifs c’est augmenter la vitesse de la réaction ». Une agitation efficace améliore la cinétique de réaction et la cinétique de transfert d’espèces chimiques d’une phase à une autre (extraction liquide-liquide), améliore la dispersion d’une ou plusieurs phases dans une autre (exemple : dispersion homogène d’un gaz dans un liquide formant des bulles très fines) et le transfert thermique. Un mauvais mélange peut engendrer des réactions secondaires, des dégradations et même pas de réaction du tout.
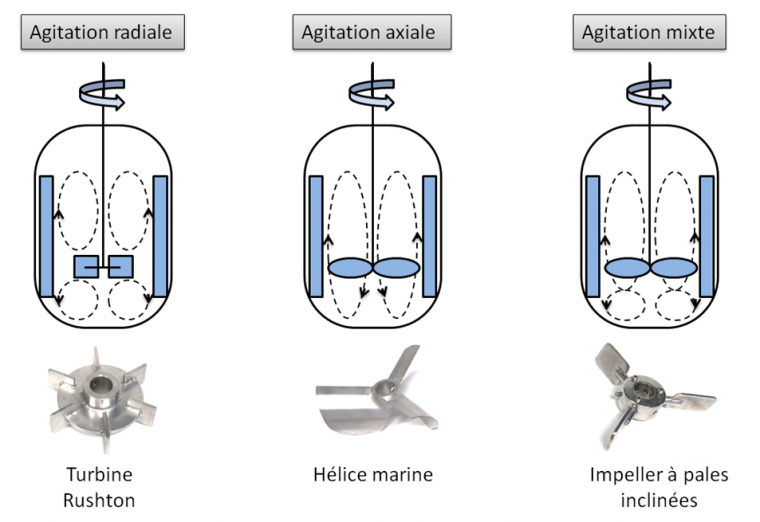
Les types de mobiles d’agitation doivent être adaptés à ce qu’on cherche à faire et les dizaines de modèles de chaque type ne se valent pas (Figure 4).
Une cristallisation, une réaction en conditions biphasiques liquide-liquide, liquide-solide, ou liquide-gaz se feront avec des mobiles différents. Par exemple, une turbine type Rushton est certes très énergivore, mais permet de disperser très finement deux phases pour des extractions liquide-liquide (augmentation de la surface de contact des deux phases). Ce mobile ne sera cependant pas adapté à une cristallisation, car il a un effet cisaillant qui casse les cristaux formés. Une hélice sera efficace pour des réactions solide-liquide car elle empêche le dépôt de solide au fond du réacteur en le faisant transiter dans tout le réacteur. Il est important de noter que tous ces mobiles d’agitations ne sont efficaces que si des chicanes sont présentes dans le réacteur (voir Figure 2) : elles sont soudées à la paroi interne du réacteur et elles servent à éviter la formation d’un vortex lié à la rotation de l’arbre d’agitation et transforme le mouvement tangentiel du milieu réactionnel en un mouvement multidirectionnel.
Conclusion
Vous avez pu découvrir dans cet article certaines facettes notre métier : le développement chimique, qu’il soit mis en œuvre dans une industrie pharmaceutique ou chimique, est un domaine passionnant. Bien sûr, le développement chimique ne se résume pas seulement à ces quelques lignes, c’est un domaine très complexe et le maîtriser demande des années d’expérience.
Pour mener à bien le développement industriel d’un procédé de fabrication d’un médicament, les équipes de chimistes s’appuient sur les compétences d’analystes, dont la mission est de développer les méthodes analytiques et les spécifications du médicament, d’experts en sécurité des procédés, en cristallisation ou en développement technologique et sur celles des opérateurs de l’atelier pilote.
Nous espérons que cet article vous donnera l’envie d’aller plus loin dans la découverte de ce métier encore assez peu connu des étudiants. Si tel est le cas, des ouvrages complets et très détaillés sont disponibles, par exemple : Practical Process Research & Development (de Neil G. Anderson, Academic press) et The Pilot Plant Real Book (Francis McConville, FXM Engineering and design). N’hésitez pas également à nous contacter directement.
A bientôt !
À propos de Servier et d’ORIL Industrie
Servier est un laboratoire pharmaceutique international gouverné par une Fondation, et dont le siège se trouve à Suresnes (France). S’appuyant sur une solide implantation internationale dans 148 pays et sur un chiffre d’affaires de 4 milliards d’euros en 2016, Servier emploie 21 000 personnes dans le monde. La croissance du groupe repose sur la recherche constante d’innovation dans cinq domaines d’excellence : les maladies cardiovasculaires, le diabète, les cancers, les maladies immuno-inflammatoires et les maladies neurodégénératives, ainsi que sur une activité dans les médicaments génériques de qualité. Étant totalement indépendant, le Groupe réinvestit 25 % de son chiffre d’affaires hors génériques en Recherche et Développement et utilise tous ses bénéfices au profit de sa croissance.
ORIL Industrie (Organisation de la Recherche Industrielle de Laboratoire) est la branche de chimie fine du groupe Servier depuis 1965. ORIL fabrique les 22 principes actifs Servier et dispose d’un Centre de Recherche Industrielle (CRI) comprenant 170 personnes et 7 entités opérationnelles : le Développement Chimique, le Développement Analytique, les Spécialités, le Pilote, les Projets, le département ARQ (Affaires Réglementaires et Qualité) et la sous-traitance.