La notion d'atome est donnée pour la première fois par Démocrite entre -460 et -370 avant J.C, qui le définit comme la plus petite partie insécable d'un corps simple. Il faudra cependant attendre le XIXème siècle pour que l'atome passe d'un concept philosophique à un concept scientifique. Ce n'est qu'au début du XXème siècle que l'on aura les moyens techniques pour sonder la matière à l'échelle subatomique. L'expérience de Rutherford joue un rôle déterminant car elle met en évidence le caractère lacunaire de la matière.
Présentation
La notion d'atome est donnée pour la première fois par Démocrite entre -460 et -370 avant J.C. Il le définit comme la plus petite partie insécable d'un corps simple.
Il faudra cependant attendre le XIXème siècle, avec notamment J. Dalton et A. Avodagro pour que l'atome passe d'un concept philosophique à un concept scientifique. Ce n'est qu'au début du XXème siècle que l'on aura les moyens techniques pour sonder la matière à l'échelle subatomique.
Contexte scientifique
La notion d'électron, ou "atome d'électricité", est posée par G. Stoney. La démonstration expérimentale ainsi que la caractérisation de cette particule viendront avec J.J. Thomson. Celui-ci prouve que la matière est constituée de lourdes parties positives et d'électrons, parties négatives plus légères, pour lesquelles il arrive à déterminer la charge et la masse.
J.J. Thomson entrevoit ainsi la notion d'atomes sécables. Pour respecter la vision classique de la matière continue, il propose le modèle du "plum-pudding".

Il imagine que les électrons, le "plum" se déplacent dans un milieu chargé positivement : le "pudding".
La découverte, dans le même temps par Henri Becquerel de la radioactivité, est une étape décisive. En effet, Ernest Rutherford, ancien élève de J.J. Thomson, se lance dans ce nouveau domaine et identifie les rayonnements α et β, en les distinguant selon leur pénétrabilité. Il montre que la radioactivité α émet des particules : des noyaux d'Hélium.
L'expérience de Rutherford
Pour étudier plus précisément le rayonnement α, Ernest Rutherford propose en 1909 de bombarder une feuille d'or avec ces particules en plaçant un écran de détection tout autour de la feuille d'or.
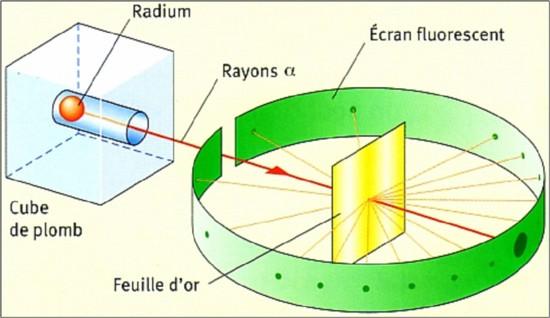
Le scintillement lumineux observé sur l'écran permet de visualiser la collision par les particules α. Au lieu de la répartition statistique gaussienne attendue avec la théorie du "plum-pudding", l'expérience montre que la plupart des particules traversent la feuille d'or sans déviation. Ernest Marsden et Hans Geiger découvrent en affinant cette technique que des particules α (1 sur 8000) sont déviées avec un angle supérieur à 90° [1].
Cette expérience met en évidence le caractère lacunaire de la matière et montre que les charges positives de l'atome sont fortement localisées dans l'espace. Ernest Rutherford propose alors un modèle en accord avec cette observation : le modèle planétaire.
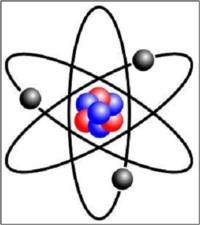
Il postule une représentation lacunaire de la matière où les électrons sont satellisés autour d'un noyau chargé positivement.
Critiques et perspectives
Cependant ce modèle n'est pas en accord avec les lois de l'électromagnétisme. En effet, l'électron sur son orbite est radialement accéléré et devrait donc rayonner selon la loi de Larmor. Ceci impliquerait une perte de l'énergie totale de l'électron, qui s'écraserait alors sur le noyau. De plus, ce modèle n'explique absolument pas la série de Balmer du spectre de l'hydrogène.
Niels Bohr propose alors, en s'inspirant des travaux de Max Planck, que le moment cinétique de l'électron est un multiple entier de h. Ainsi l'électron ne peut rayonner car on lui impose une énergie sur une orbite donnée. Ce modèle, qui règle le problème de l'instabilité du modèle planétaire, permet également de retrouver la série de Balmer.
Par la suite, le modèle de Bohr sera justifié par la mécanique quantique dans le cas particulier des hydrogénoïdes [2]. Il n'est pas valable dans les autres cas, car Niels Bohr postulait une orbite sphérique.
Les problèmes posés par le modèle planétaire de Ernest Rutherford font état de l'impossibilité de modéliser l'atome de manière satisfaisante grâce à la mécanique classique. Néanmoins, la mécanique quantique restant obscure pour le plus grand nombre, le modèle planétaire demeure la représentation traditionnelle dans l'imaginaire populaire.
Bibliographie et ressources en ligne
[1] H. Geiger and E. Marsden, On a Diffuse Reflection of the alpha-Particles, Compte rendu de la Royal Society, 1909 A vol. 82, p. 495-500
[2] Un article de CultureSciences-Chimie autour des atomes hydrogénoïdes et de l'approximation orbitalaire : Orbitales atomiques - approximation orbitalaire
[3] Un article de CultureSciences-chimie : Le modèle de Bohr