Les organismes vivants sont sources d’inspiration pour l’homme depuis des siècles, de Léonard de Vinci à l’inventeur du Velcro®. L’étude présentée ici s’inscrit dans cette continuité. Elle applique cette démarche au stockage électrochimique de l’énergie avec une légère différence : il ne s’agit plus de s’inspirer de la nature mais d’apprendre à en tirer directement bénéfice.
Présentation
Une équipe de chercheurs du Laboratoire de réactivité et chimie des solides (CNRS / Université de Picardie) en collaboration avec des chercheurs de l’Institut de minéralogie et de physique des milieux condensés (CNRS / UPMC) vient d’utiliser des bactéries pour produire des coques d’oxyde de fer utilisables comme matériaux d’électrodes pour batteries Li-ion. Ces résultats font l’objet d’une publication dans la revue Energy & Environmental Science.
Les électrodes des batteries Li-ion
La technologie Li-ion repose sur une chimie riche liée à la large gamme de matériaux qui peuvent être utilisés comme électrodes positives (LCO, LFP, NMC, LMO…) et négatives (C, Sn, Si, LTO…). Actuellement, la plupart de ces matériaux d’électrode commerciaux sont préparés par voie céramique (T > 400 °C) avec de longues périodes de chauffe (> 24h). Ils ont donc un coût énergétique élevé. Les scientifiques étudient donc de plus en plus de nouvelles voies de synthèse durables moins énergivores (ex : « chimie douce »). En France, le réseau de recherche sur le stockage électrochimique de l’énergie (RS2E) regroupe les équipes qui développent cette thématique liée au « stockage éco-compatible ».
Dans ce contexte, une équipe du réseau RS2E vient de mettre au point la synthèse d’un oxyhydroxyde de fer par voie bactérienne à température ambiante. La bactérie utilisée, Acidovorax sp., mesure 1 à 2 µm de long et 0,2 µm de large. Par son métabolisme elle peut remplir son périplasme, un espace de 40 nm d’épaisseur situé entre les deux parois de sa membrane, avec des cristaux de gamma-FeOOH (la lépidocrocite, un oxyhydroxyde de fer solide cristallisé). Il est ensuite possible de transformer la lépidocrocite présente dans le périplasme en hématite par un chauffage court (< 1h) à 700°C qui détruit également la bactérie (fig. 1). Le choix de l’hématite (α-Fe2O3) est motivé par sa forte capacité à stocker des charges électriques (1000 mAh/g).
Des coques d'oxyde de fer durables
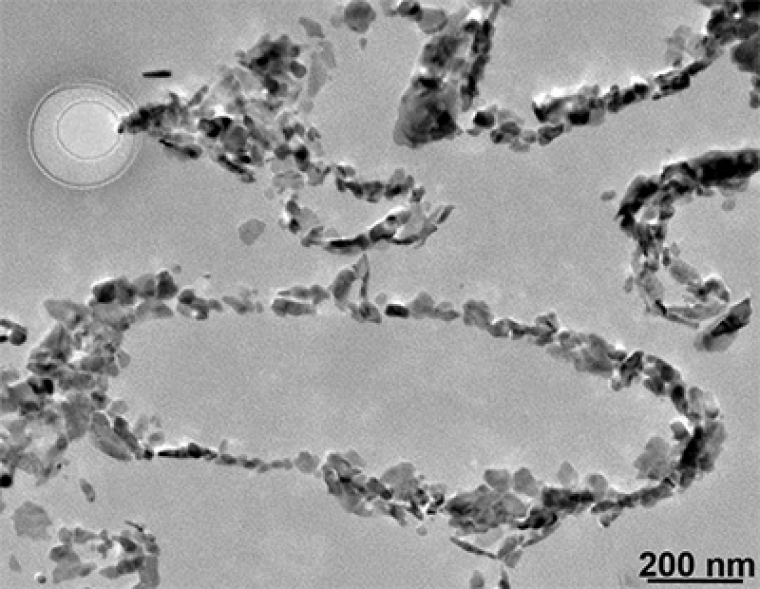
La poudre d’hématite ainsi produite est organisée sous forme de multiples coques creuses reprenant la forme du périplasme des bactéries, qui ont agi comme des moules (fig. 2). Les chercheurs ont utilisé le terme « bactériomorphes » pour désigner ces coques.
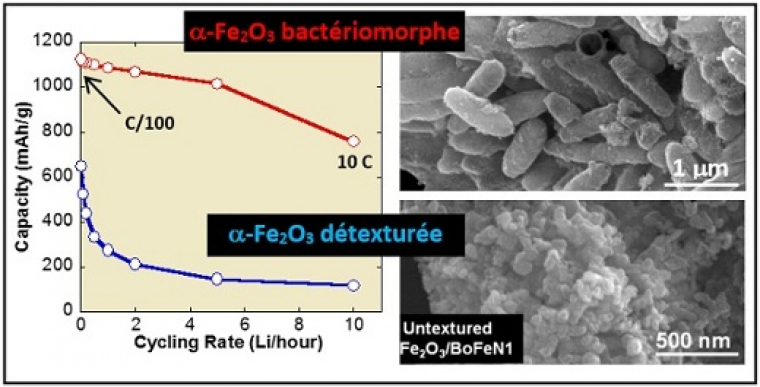
Cette organisation particulière confère-t-elle des propriétés intéressantes à l’hématite ? Pour répondre à cette question, les chercheurs ont comparé les performances de cette hématite organisée sous forme de coques creuses à des bactériomorphes d‘hématite détexturés (broyés pour détruire leur organisation en coques creuses) et à de l’hématite abiotique (synthétisée par voie chimique « classique »).
Après 10 cycles de charges-décharges à vitesse lente, 91 de la capacité initiale à stocker des charges demeure. Elle n’est que de 18 % pour les échantillons abiotiques, et de 8 % pour ceux qui sont détexturés (fig. 3). Encore plus surprenant, les coques conservent cette aptitude de stockage sur une vaste gamme de vitesses de charge/décharge. En effet, si l’on fait varier cette vitesse de charge-décharge d’un facteur 1000 (entre C/100 et 10C), 70 % de l’aptitude initiale à stocker des charges est conservée. Cette excellente capacité de stockage s’explique par l’organisation micrométrique des coquilles bactériomorphes qui confère une meilleure stabilité mécanique à l’électrode et par une porosité qui permet un meilleur contact avec l’électrolyte.
Perspectives
À ce jour, ces nouvelles électrodes comptent parmi les plus performantes obtenus avec de l’hématite. Ces travaux ont permis aux chercheurs de mettre l’accent sur l’obtention de propriétés électrochimiques remarquables liées à une organisation originale du matériau obtenu par une voie de synthèse moins coûteuse en énergie. Par ailleurs, l’utilisation à grande échelle de bactéries comme moyen de production est déjà maîtrisée, par exemple pour produire de l’insuline ou du glutamate. On compte ainsi 2 millions de tonnes de glutamate produites par an de cette façon.
Les scientifiques veulent maintenant dépasser le stade de l’étude en produisant par voie bactérienne des matériaux d’électrodes positives directement utilisables dans des systèmes Li-ion tels que les phosphates doubles (formule générale AMPO4 où A est un métal alcalin – Li, Na… – et M un métal de transition 3d – Fe, Mn…).
Bibliographie et Ressources en Ligne
- J. Miot, N. Recham, D. Larcher, F. Guyot, J. Brest et J-M. Tarascon Biomineralized α-Fe2O3 : Texturation and electrochemical reaction with Li. Energy & Environmental Science, 7 Novembre 2013.
- Vers une chimie douce bio-inspirée par Jacques Livage, Professeur au Collège de France, publié sur CultureSciences-Chimie.
- Une pile à hydrogène bio-inspirée par Christophe Cartier dit Moulin, publié sur CultureSciences-Chimie.
- Oxydation ménagée : vers une valorisation bio-inspirée du méthane ? Par Christophe Cartier dit Moulin et Martine Hasler, publié sur CultureSciences-Chimie.
Article rédigé à partir de celui de Dominique Larcher et al. (Chercheurs au Laboratoire de réactivité et chimie des solides – Amiens) sur leurs travaux.