Le premier article du dossier sur les nanoparticules d'or se concentre sur les propriétés surprenantes de ces objets. On y apprend notamment que l'or aussi peut rougir !
Introduction
De tout temps, l’or a été source de fascination à l’état macroscopique de par son incroyable couleur dorée, sa rareté, ses propriétés électroniques, ainsi que sa résistance dans le temps grâce à son caractère inoxydable. C’est seulement à partir des années 1980 que le monde de la recherche scientifique commence à s’intéresser de près à l’or sous la forme nanométrique, qui possède des propriétés physico-chimiques totalement différentes de celles de l’état massif. En effet, l’or de taille nanométrique n’est plus doré mais peut prendre différentes couleurs dans le domaine du visible, du bleu jusqu’au rouge en fonction de sa taille et de sa forme. De plus, à l’échelle nanométrique, le potentiel d’oxydo-réduction de l’or devient bien plus négatif qu’à l’état massif, ce qui peut entraîner de nouvelles applications en catalyse par exemple. Les propriétés physiques du métal diffèrent également : alors que l’or massif fond à 1063°C, une nanoparticule d’or mesurant 2,5 nm de diamètre fond à 300°C ! Et encore : à l’échelle nanométrique, l’or devient biodégradable. Toutes ces nouvelles propriétés ont permis aux particules d’or de se hisser au plus haut dans la recherche en nano-sciences. Cet article a pour objectif de comprendre la synthèse des nanoparticules d’or, d’expliquer leurs propriétés optiques et de comprendre pourquoi celles-ci ont un avenir très prometteur dans l’imagerie médicale et comme nano-médicaments, utilisés notamment dans la lutte contre le cancer.
Bien que l’étude et la compréhension des nanomatériaux soient relativement récentes, des objets de l’antiquité romaine ont révélé que les romains utilisaient déjà l’or sous forme de nanoparticules dans des colorants qu’ils incorporaient à des œuvres d’art comme la sur- prenante coupe de Lycurgue qui date du IVe siècle après J.C.. Cette coupe est célèbre pour ses incroyables propriétés optiques comme on peut le remarquer sur la Figure 1. Si la coupe est éclairée par une lumière qui est réfléchie, alors celle-ci parait verte. En revanche, lorsqu’on observe la coupe par une lumière en transmission, alors elle apparait rouge.
D'après Rosamund Daw, Nanotechnologies, déjà dans l’Antiquité..., Courrier Sciences, 2013.
Ce n’est que dans les années 1990 que des chercheurs ont montré que ces phénomènes optiques étaient dus à la présence de nanoparticules d’or-argent sous forme d’alliage avec un peu de cuivre.
Comment expliquer ces étonnantes propriétés optiques que possèdent les nanoparticules d’or ? Comment synthétiser et caractériser ces nanoparticules ? Et quelles sont les utilisations de ces nanomatériaux ?
Propriétés optiques des nanoparticules d’or : pourquoi l’or devient rouge lorsqu’il a une taille nanométrique ?
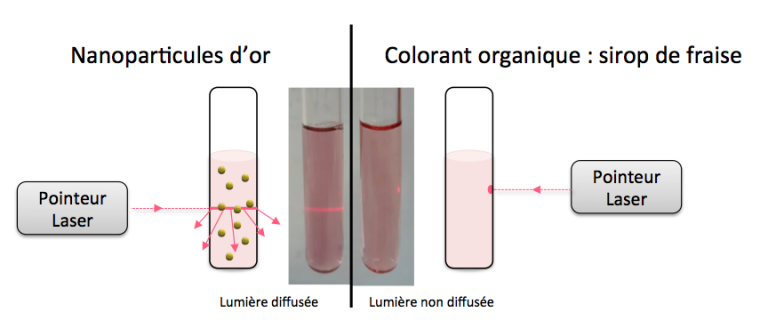
Les nanoparticules d’or sont de tout petits solides qui peuvent être dispersés en solution (aqueuse ou organique), il s’agit donc d’une suspension qui est appelée « suspension colloïdale inorganique ». Bien qu’à l’oeil nu il soit impossible de distinguer un colorant organique dissout en solution et une suspension colloïdale de nanoparticules solides, il est toutefois possible de mettre en évidence la présence des nanoparticules avec un simple pointeur laser. En éclairant la suspension colloïdale avec le laser, il sera possible de voir la trajectoire du laser à l’intérieur de la solution alors que ceci sera impossible avec le colorant. Ceci est dû à la diffusion de la lumière par les nanoparticules qui sont beaucoup plus grosses que les molécules organiques du colorant. Ce phénomène de diffusion des nanoparticules est montré en Figure 2. A gauche se trouve une suspension colloïdale de nanoparticules d’or d’environ 10 nm de diamètre. A droite se trouve du sirop de fraise : cette fois-ci la couleur est due à la présence d’un colorant organique. Il est à noter que la solution contenant les particules d’or est ici 37 000 fois moins concentrée que la solution de sirop de fraise alors que les deux tubes ont une couleur de même intensité ! Les particules d’or sont donc très colorées (c’est-à-dire qu’elle absorbent fortement la couleur complémentaire).
Cette très simple expérience permet d’observer de façon indirecte la présence de solides en solution mais n’explique toujours pas les propriétés optiques de l’or sous forme nanométrique.
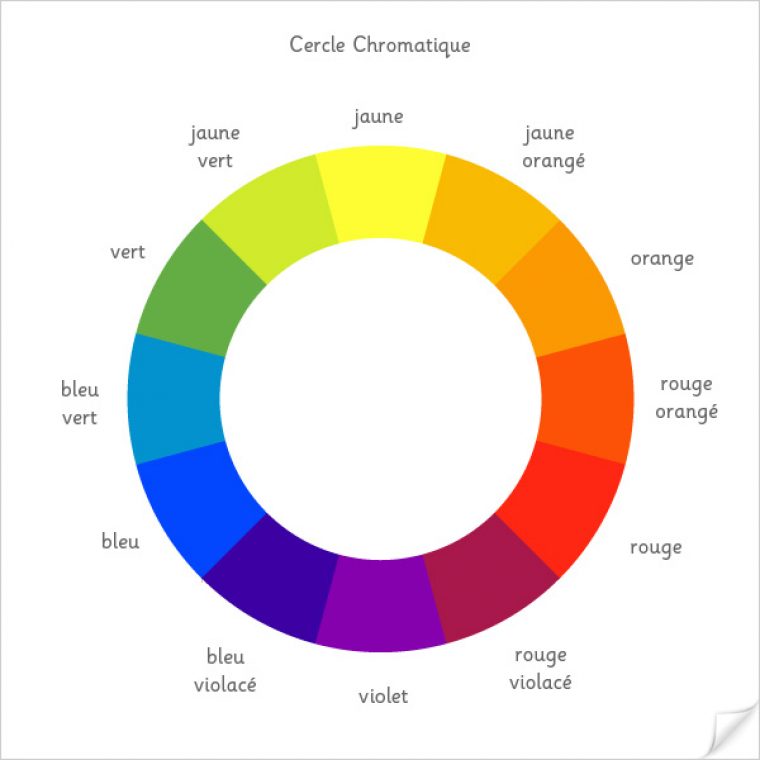
Les nanoparticules d’or sphériques en suspension colloïdale ne sont pas de couleur dorée mais sont plutôt rouges comme observé sur la figure précédente. Cela signifie qu’elle absorbent la lumière complémentaire à la couleur rouge, à savoir le vert.
Des couleurs complémentaires sont diamétralement opposées sur le cercle chromatique.
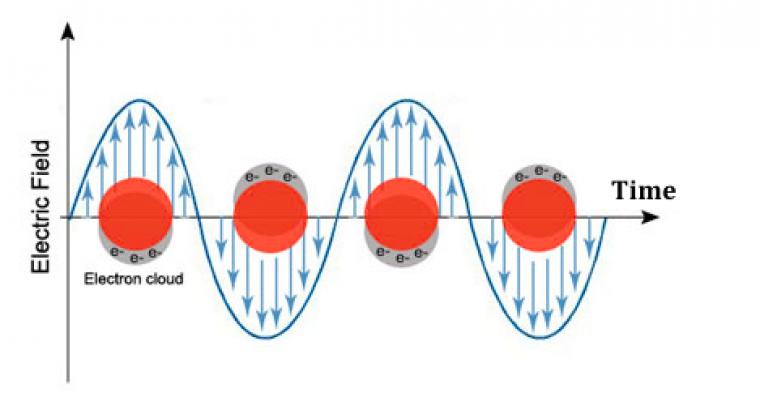
Cette absorbance provient d’une oscillation collective des électrons présents à la surface des particules sous l’effet d’un rayonnement électromagnétique (ici de la lumière visible). En effet, lorsqu’une particule métallique est soumise à un champ électromagnétique dont la longueur d’onde est beaucoup plus grande que le taille des particules, tous les électrons libres de la bande de conduction subissent le même champ et oscillent collectivement en phase. Lorsque la fréquence de l’onde incidente correspond à la fréquence propre de ces oscillations, il se produit un phénomène de résonance, appelé plasmon de surface ou fréquence de résonance plasmon. Ce phénomène est schématisé sur la Figure 4. Lorsque la fréquence de l’onde lumineuse incidente est égale à la fréquence de résonance de l’or, il y a alors une très forte absorption de cette onde incidente.
La fréquence de résonance plasmon va varier en fonction de la nature du métal, de la taille, de la forme et l’état de surface de la nanoparticule. Seul l’or, l’argent et le cuivre possèdent des résonances plasmoniques dans le domaine du visible. Dans le cas de l’or, la résonance plasmon se trouve vers 520 nm donc les nanoparticules d’or vont fortement absorber cette lumière verte et la couleur observée sera donc la couleur complémentaire : le rouge. Plus les nanoparticules sphériques seront grandes, plus le pic plasmonique sera décalé vers les grandes longueurs d’onde (effet bathochrome) et donc la couleur de la solution de nanoparticules sera modifiée comme cela peut être observé sur la Figure 5.
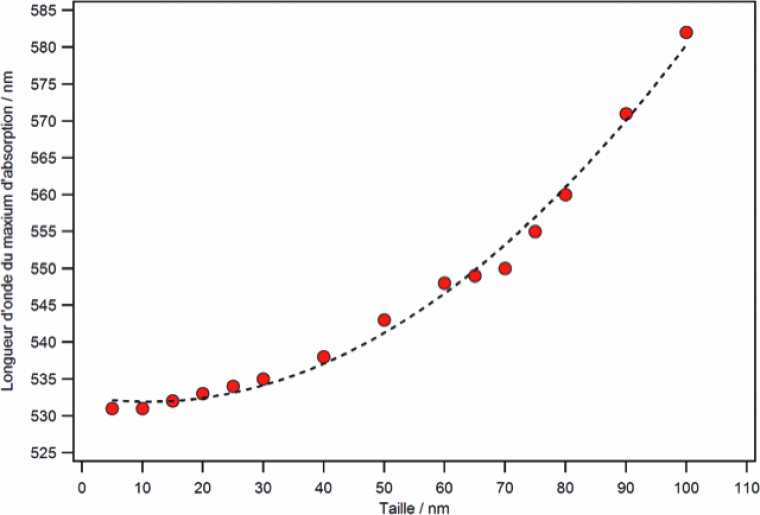
Il n’existe pas de relation analytique simple permettant d’obtenir la position de la résonance plasmon en fonction de la taille de la nanoparticule d’or. Cependant, une courbe d’étalonnage calculée numériquement (réalisée via le logiciel MiePlot et présentée dans le BUP n° 952) est représentée sur la Figure 6.
Figure extraite de l'article J. Piard, F. Maisonneuve, C. Allain et D. Schaming, « Synthèse et détermination de la taille de nanoparticules d'or », Bull. Un. Prof. Phys. Chim., vol. 107, n° 952, p. 327-339, mars 2013 du BUP n°952
Bibliographie et Références
- L’or nanométrique, un agent thérapeutique, Actualité Chimique n°425, Janvier 2018.
- Bienvenue dans le monde de l’or Nanométrique ! Actualité Chimique n°425, Janvier 2018.
- Nanoparticules d’or, Technique de L’ingénieur, NM900V1, 10 Janvier 2011.
- Synthèse et détermination de la taille de nanoparticules d’or, BUP 952, Vol. 107, Mars 2013.
- Nanoparticules d'or pour la santé
- Rosamund Daw. Nanotechnologies, déjà dans l’Antiquité... Courrier Sciences, 2013.
- Victor K LaMer and Robert H Dinegar. Theory, production and mechanism of formation of monodispersed hydrosols. Journal of the American Chemical Society, 72(11):4847– 4854, 1950.
- J Kimling, M Maier, B Okenve, Vassilios Kotaidis, H Ballot, and Anton Plech. Turkevich method for gold nanoparticle synthesis revisited. The Journal of Physical Chemistry B, 110(32):15700–15707, 2006.
- Stephan Link, MB Mohamed, and MA El-Sayed. Simulation of the optical absorption spectra of gold nanorods as a function of their aspect ratio and the effect of the medium dielectric constant. The Journal of Physical Chemistry B, 103(16):3073–3077, 1999.
- Xingchen Ye, Chen Zheng, Jun Chen, Yuzhi Gao, and Christopher B Murray. Using binary surfactant mixtures to simultaneously improve the dimensional tunability and monodispersity in the seeded growth of gold nanorods. Nano letters, 13(2):765–771, 2013.
- Xingchen Ye, Linghua Jin, Humeyra Caglayan, Jun Chen, Guozhong Xing, Chen Zheng, Vicky Doan-Nguyen, Yijin Kang, Nader Engheta, Cherie R Kagan, et al. Improved size- tunable synthesis of monodisperse gold nanorods through the use of aromatic additives. ACS nano, 6(3):2804–2817, 2012.
- Erik C Dreaden, Alaaldin M Alkilany, Xiaohua Huang, Catherine J Murphy, and Mostafa A El-Sayed. The golden age: gold nanoparticles for biomedicine. Chemical Society Reviews, 41(7):2740–2779, 2012.
- Mohammad Eghtedari, Alexander Oraevsky, John A Copland, Nicholas A Kotov, Andre Conjusteau, and Massoud Motamedi. High sensitivity of in vivo detection of gold nanorods using a laser optoacoustic imaging system. Nano letters, 7(7):1914–1918, 2007.