Ce troisième et dernier article du dossier sur les nanoparticules d'or se concentre sur les diverses applications des nanoparticules d'or, en particulier dans le domaine médical.
Le lecteur est invité à se référer aux premier et deuxième articles du dossier, qui présentent les propriétés, ainsi que quelques synthèses de ces objets d'intérêt.
Fonctionnalisation des nanoparticules d’or
Si l’on souhaite utiliser des nanoparticules d’or pour du diagnostic médical ou bien comme agent thérapeutique, il est nécessaire que ces dernières soient biocompatibles. Pour cela, les ligands (ou agents stabilisants) accrochés à la surface des particules jouent un rôle crucial. En effet, il est nécessaire que les ligands ne se décrochent pas de la surface des particules mais aussi qu’ils permettent une excellente stabilisation colloïdale des particules d’or dans des milieux biologiques. Les surfaces d’or sont faciles à fonctionnaliser par des fonctions thiols ou des fonctions amines via des liaisons de coordination. Le choix de l’agent stabilisant peut être fait au moment de la synthèse ou par échange de ligands après la synthèse (post-fonctionnalisation). Cet agent stabilisant doit être un ligand bifonctionnel, c’est-à-dire qui contient une fonction qui servira d’accroche sur les nanoparticules et une fonction hydrophile permettant la solubilisation dans l’eau.
Etude d’un exemple :
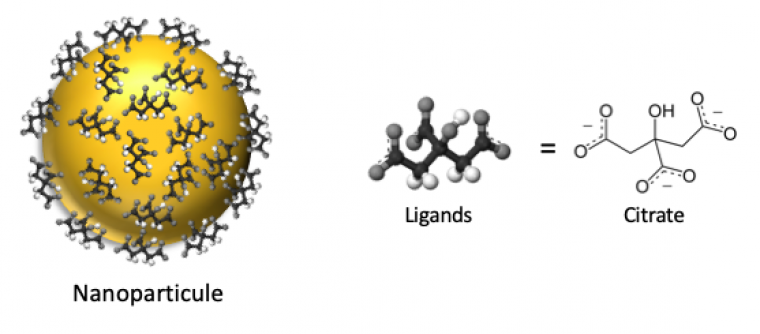
Les nanoparticules d’or sphériques présentées précédemment sont stabilisées en surface par l'ion citrate (Figure 1), qui est chargé négativement.
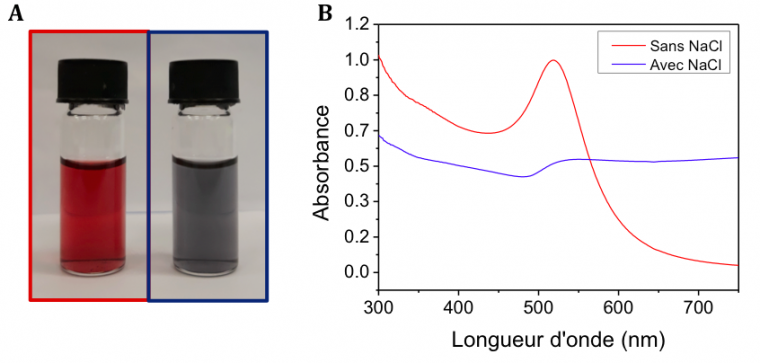
Les nanoparticules se repoussent entre elles et ne s’agrègent pas grâce à la répulsion électrostatique. Si on ajoute à cette suspension du chlorure de sodium (NaCl), alors les ions sodium chargés positivement vont venir écranter les charges de surface des nanoparticules. Les nanoparticules s’agrégent alors et un changement de couleur est observable : la solution passe de rouge à bleue. Cette agrégation, irréversible, pose un problème si l’on souhaite utiliser ces particules dans le domaine de la médecine car le sang contient une concentration saline relativement élevée. Pour pallier ce problème, il est possible de faire des échanges de ligands à la surface des particules d’or. On peut, par exemple, ajouter des ligands avec fonctions thiols comme le PEG-SH (polyéthylène glycol avec un thiol terminal) ou un alkyl-thiol. Les thiols ont une très forte affinité avec l’or et déplacent les ions citrate. Cette fois-ci, les nanoparticules d’or sont stabilisées grâce à une répulsion stérique et non plus électrostatique. L’ajout de sel ne modifiera pas la stabilité colloïdale.
L’or nanométrique : un agent pour le diagnostic, l’imagerie et la thérapie
Agent thérapeutique : délivrer un médicament
Les nanoparticules d’or peuvent être utilisées en biologie pour l’imagerie et pour le diagnostic. Elles peuvent aussi vectoriser des substances actives comme des médicaments vers des cibles (organes, cellules...). Grâce à leur forte absorbance plasmonique, les nanoparticules d’or présentent un fort potentiel dans le domaine de la thérapie. Une des techniques de reconnaissance des cellules cancéreuses est l’utilisation de nanoparticules "décorées" de molécules de reconnaissance des cellules cancéreuses tels que des anticorps ou des ligands de type sucre. Dans le milieu biologique, ceux-ci peuvent reconnaître les antigènes ou les récepteurs des cellules cancéreuses et ainsi envoyer les nanoparticules plus spécifiquement vers ces cellules. Si les particules d’or transportent des composés thérapeutiques, elles peuvent alors les déposer spécifiquement dans les cellules cancéreuses.
Agent thérapeutique : les nanoparticules d’or peuvent détruire les cellules cancéreuses
En fait, les particules d’or peuvent même à elles seules réussir à détruire des cellules cancéreuses par photothermie ! En effet, la photothermie est l’une des applications les plus prometteuses dans l’utilisation des particules d’or pour la lutte contre le cancer. Grâce à leur absorbance plasmonique, les particules d’or peuvent absorber énormément d’énergie (à la longueur d’onde qui correspond à leur absorbance maximale) et la convertir en chaleur. Par conséquent, une fois les nanoparticules d’or fixées dans les tissus cancéreux, il suffit de les éclairer avec un laser à leur fréquence plasmonique et un fort dégagement de chaleur sera alors créé. Cela entraîne des lésions irréversibles dans les cellules cancéreuses ce qui conduit à leur mort. Cette technique est très prometteuse et actuellement testée dans plusieurs essais cliniques.
Agent pour l'imagerie en photoacoustique
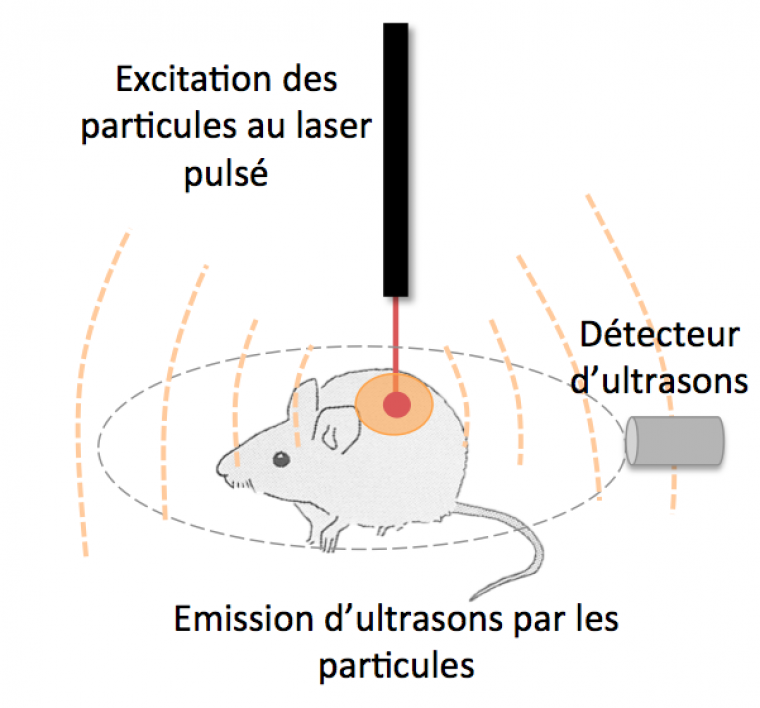
Les nanoparticules d’or peuvent aussi permettre de repérer les cellules cancéreuses par imagerie photoacoustique. L’imagerie photoacoustique, en tant que modalité de l’imagerie biomédicale, est basée sur l’effet photoacoustique [9]. Dans l’imagerie photoacoustique, des impulsions laser non-ionisantes sont envoyées dans les tissus biologiques dans lesquels des particules d’or sont préalablement injectées. Ces particules ont la capacité d’absorber une partie de cette lumière et de créer un fort dégagement de chaleur. Par conséquent, une partie de l’énergie émise par le laser est alors convertie en chaleur. Cette augmentation locale de la chaleur crée une dilatation des tissus. Ces derniers subiront des cycles de dilatation-compression générant des ondes mécaniques qui peuvent alors être détectées et analysées pour construire une image interne du patient. L’amplitude de l’émission d’ultrasons est proportionnelle à l’absorption optique. Les tissus biologiques n’ayant pas la même absorption optique, il est possible de réaliser des images 2D ou 3D de la zone ciblée. Les particules d’or, et plus particulièrement les nanobâtonnets d’or, ont une très forte absorbance plasmonique, c’est pourquoi ils sont d’excellents candidats comme agents de contraste en imagerie photoacoustique. En effet, les nanobâtonnets d’or sont capables de convertir plus de 90% des photons absorbés en chaleur grâce à des processus de désexcitation non radiatifs. Il est alors possible de repérer par imagerie photoacoustique l’emplacement des nanobâtonnets d’or in vivo.
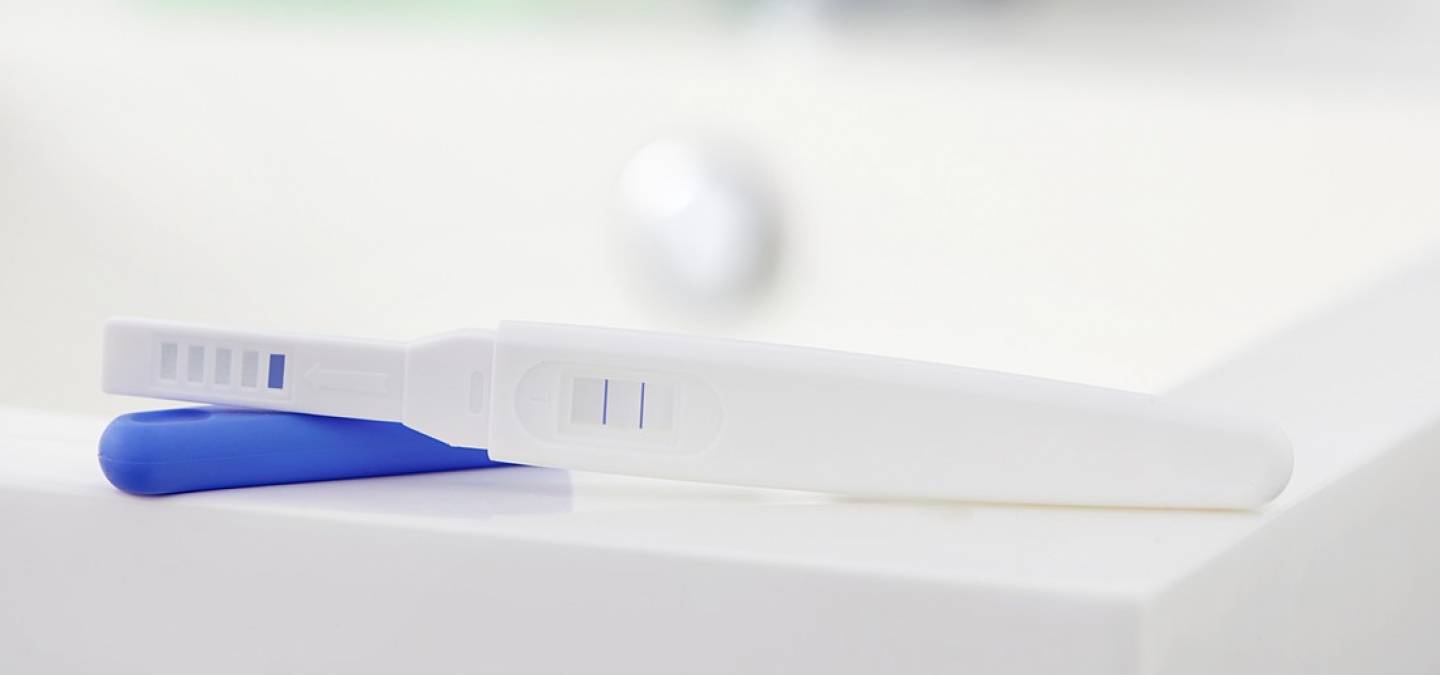
Les nanoparticules d’or pour le diagnostic : les tests de grossesse
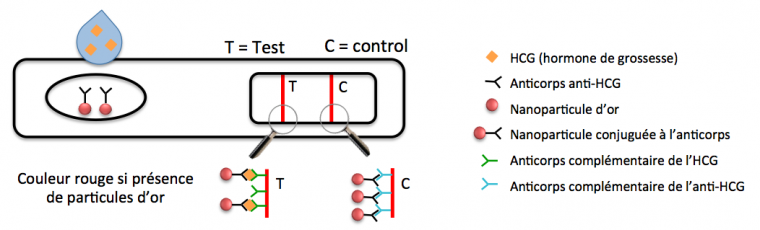
Les nanoparticules d’or peuvent aussi servir pour des test de diagnostic ou tests de dépistage rapide ; par exemple, elles sont utilisées dans certains tests de grossesse. Comme nous l’avons vu en dans le 1er article du dossier, les suspensions colloïdales concentrées de nanoparticules d’or sont très colorées même à faible concentration. Il est donc possible de les utiliser pour des tests visuels en utilisant leur couleur. Le principe du test de grossesse est de détecter dans l’urine la présence d’une hormone produite uniquement au cours d’une grossesse, l’hormone chorionique gonadotrophique, notée bêta-HCG. Il est possible d’utiliser pour cela des nanoparticules d’or fonctionnalisées en surface par des anticorps anti-bêta-HCG. Lorsque l’hormone de grossesse est présente dans l’urine, les nanoparticules d’or vont alors se lier à cette dernière via l’anticorps. Lors de la réalisation du test de grossesse, l’urine entraîne les particules d’or qui sont retenues sur la bande test (bande T voir Figure 2) uniquement si il y a présence de la bêta-HCG. Ceci crée une bande rouge colorée qui correspond à l’accumulation des particules. En réalité, dans les tests de grossesse, il y a toujours deux bandes observées : une bande liée à la présence de l’hormone (la bande test), la deuxième bande étant simplement une bande de contrôle permettant de vérifier que le test a été correctement réalisé.
Conclusion
La recherche autour des nanoparticules connaît un véritable engouement. Les recherches effectuées jusqu’à ce jour ont permis de comprendre et d’utiliser de tout nouveaux matériaux ayant des propriétés physiques et chimiques totalement différentes de celles connues jusqu’alors grâce à leur petite taille ! Les nanoparticules d’or sont particulièrement intéressantes car elles présentent des applications dans de très nombreux domaines tels que l’optique, l’électronique, la catalyse, la biologie et la médecine.
Au sein de ce dossier, le diagramme de La Mer a permis de mieux comprendre les différentes étapes de formation des nanoparticules. Les propriétés physiques de résonance plasmonique des particules d’or ont été expliquées, ce qui a permis de comprendre leurs propriétés optiques. Deux synthèses de nanoparticules d’or ayant des formes différentes (sphère et bâtonnet) ont été expliquées et les protocoles détaillés. Pour finir, quelques exemples d’utilisation de nanoparticules d’or dans le domaine de la santé ont été présentés.
Les nanoparticules connaissent un tel essor dans le monde de la recherche scientifique qu’il est fort probable que celles-ci fassent encore longtemps parler d’elles !
Bibliographie et Références
- L’or nanométrique, un agent thérapeutique, Actualité Chimique n°425, Janvier 2018.
- Bienvenue dans le monde de l’or Nanométrique ! Actualité Chimique n°425, Janvier 2018.
- Nanoparticules d’or, Technique de L’ingénieur, NM900V1, 10 Janvier 2011.
- Synthèse et détermination de la taille de nanoparticules d’or, BUP 952, Vol. 107, Mars 2013.
- Nanoparticules d'or pour la santé
- Rosamund Daw. Nanotechnologies, déjà dans l’Antiquité... Courrier Sciences, 2013.
- Victor K LaMer and Robert H Dinegar. Theory, production and mechanism of formation of monodispersed hydrosols. Journal of the American Chemical Society, 72(11):4847– 4854, 1950.
- J Kimling, M Maier, B Okenve, Vassilios Kotaidis, H Ballot, and Anton Plech. Turkevich method for gold nanoparticle synthesis revisited. The Journal of Physical Chemistry B, 110(32):15700–15707, 2006.
- Stephan Link, MB Mohamed, and MA El-Sayed. Simulation of the optical absorption spectra of gold nanorods as a function of their aspect ratio and the effect of the medium dielectric constant. The Journal of Physical Chemistry B, 103(16):3073–3077, 1999.
- Xingchen Ye, Chen Zheng, Jun Chen, Yuzhi Gao, and Christopher B Murray. Using binary surfactant mixtures to simultaneously improve the dimensional tunability and monodispersity in the seeded growth of gold nanorods. Nano letters, 13(2):765–771, 2013.
- Xingchen Ye, Linghua Jin, Humeyra Caglayan, Jun Chen, Guozhong Xing, Chen Zheng, Vicky Doan-Nguyen, Yijin Kang, Nader Engheta, Cherie R Kagan, et al. Improved size- tunable synthesis of monodisperse gold nanorods through the use of aromatic additives. ACS nano, 6(3):2804–2817, 2012.
- Erik C Dreaden, Alaaldin M Alkilany, Xiaohua Huang, Catherine J Murphy, and Mostafa A El-Sayed. The golden age: gold nanoparticles for biomedicine. Chemical Society Reviews, 41(7):2740–2779, 2012.
- Mohammad Eghtedari, Alexander Oraevsky, John A Copland, Nicholas A Kotov, Andre Conjusteau, and Massoud Motamedi. High sensitivity of in vivo detection of gold nanorods using a laser optoacoustic imaging system. Nano letters, 7(7):1914–1918, 2007.