Nanoparticules et nanomatériaux, qui font aujourd’hui partie du quotidien, sont l'objet d'intenses activités de recherche et d'une certaine médiatisation. Dans cet article, les notions de nanoparticules, nanotechnologies et nanosciences sont définies et l'intérêt pour cette échelle de la matière est explicité, en précisant notamment les propriétés particulières des nanoobjets. Les applications des nanoparticules à grande échelle, notamment dans le domaine de la catalyse, sont présentées.
Introduction
Depuis le 1er janvier 2013, la réglementation française impose aux producteurs, importateurs et distributeurs la déclaration des substances à l’état nanoparticulaire. Cette précaution répond à une demande forte des associations de consommateurs, et elle anticipe les réglementations européennes à venir.
Que sont ces substances à l’état nanoparticulaire, pourquoi les scientifiques s’y intéressent-ils et comment l’industrie en fait-elle usage, sont autant de questions abordées ici. Parce qu’elles brouillent les genres et les valeurs, les nanosciences et nanotechnologies interrogent. Sont-elles importantes, sont-elles nécessaires, et apportent-elles une nouvelle réponse au défi énergétique de notre siècle ?
Alors que de nombreuses études et revues font le point sur la toxicité et l’écotoxicité potentielles des nanoparticules [1], nous exposons plutôt ici les motivations à l’origine d’un changement d’échelle en recherche et développement : en quelques années seulement, les nanoparticules et nanomatériaux sont devenus un nouveau centre d’intérêt pour une large communauté de chercheurs et d’inventeurs. Pourtant, nous illustrons aussi leur usage à grande échelle – y compris industrielle : celui-ci est bien antérieur à l’émergence des « nanosciences » en tant que nouveau champ scientifique.
Nanotechnologies, nanosciences et nanoparticules
« Nano » est un préfixe tiré du mot latin nanus, signifiant « nain ». Dans le système métrique, il désigne la milliardième partie de l’unité. Initialement, ce terme ne présente donc aucune originalité par rapport aux préfixes bien connus (« kilo » pour un millier, « milli » pour un millième, etc.) : comme un centimètre est un centième de mètre et un micromètre un millionième de mètre, un nanomètre est un milliardième de mètre. Par extension, une nanoparticule est une particule d’une taille de quelques nanomètres (Figure 1). Une nanoparticule est certes petite à l’échelle humaine, mais pas « infiniment petite », comme on va le voir plus loin.
Cependant, le préfixe « nano » a servi à forger dans les années 1970 le terme Nanotechnology, suivi quelques années plus tard par l’expression Nanosciences. Le premier désigne l’ensemble des techniques et applications, alors que le second se rapporte aux questions fondamentales et aux nouvelles propriétés. Étonnamment, ces mots-slogans sont aujourd’hui très utilisés. Avait-on jamais parlé auparavant de « Milliscience » ou de « Kilotechnology » ? Proposer un champ scientifique défini par un simple paramètre d’échelle semble absurde. Comment expliquer alors le succès des deux néologismes « Nanotechnologie » et « Nanosciences » ?
Deux approches du nano
Des années 1930 aux années 1980, l’émergence de puissantes méthodes d’imagerie a permis de sonder et même de manipuler la matière à une échelle inatteignable avec un microscope optique traditionnel. Cela a suscité un très fort engouement de diverses communautés scientifiques. La fabrication et l’étude de petits objets comportant de quelques dizaines à quelques milliers d’atomes sont alors devenues un important défi. Pourtant, dès le début du XXe siècle, les outils de la chimie (synthèse organique et polymérisation) et de la biologie (synthèse peptidique) fabriquaient de manière routinière des objets de quelques nanomètres, en général à base de carbone, en assemblant de plus petites briques ou molécules (voie dite ascendante ou « bottom-up »). Ainsi, pour un chimiste, une nanoparticule, qui contient quelques milliers d’atomes, c’est un gros objet !
A gauche, le microscope électronique à balayage montre la structure 3D, en pavage hexagonal, spontanément formée par les nanoparticules. A droite, le microscope électronique en transmission révèle les nanoparticules individuelles et leur structure interne : un cœur métallique de fer gris clair, entouré d’une coquille d’oxyde de fer gris foncé.
A l’origine de la Nanotechnology se trouvent des scientifiques qui ont pris le problème à rebours. Ils ont développé de nouveaux outils pour miniaturiser la matière macroscopique traditionnelle : microscopes électronique, à effet tunnel et à force atomique1, nano-lithographie [2], etc. C’est la voie dite descendante ou « top-down » : fabriquer un objet nanométrique unique tel qu’un petit cluster d’atomes métalliques, puis l’imager et le manipuler grâce à l’outil technologique, constitue le cœur de cette nouvelle science [3]. La conjugaison d’une imagerie directe et largement appréhendable par tous, avec la manipulation télécommandée, atome par atome, de structures artificielles, a rendu concrète la notion de nanoparticule et a nourri l’imaginaire de toute une génération : nano-robots et nano-machines opérant dans notre environnement quotidien, voire même à l’intérieur du corps humain, sont les rêves phares de cette époque. En pratique, la miniaturisation des circuits imprimés, autrement dit l’augmentation exponentielle des capacités des mémoires et processeurs, constitue le grand succès technologique de ces techniques.
Cependant, la fabrication de matériaux de la vie courante nécessite souvent des méthodes plus rustiques. Même si la manipulation atomique a immensément progressé depuis 30 ans, culminant avec la réalisation du plus petit film du monde (« A Boy and His Atom » [4]), on n’arrivera probablement pas dans ce siècle à une fabrication en série de nano-robots fonctionnels avec ces outils, pour de multiples raisons. D’abord, la manipulation atomique ne donne accès qu’à un objet à la fois et requiert beaucoup de temps et d’efforts. Ensuite, les objets sont fabriqués dans des conditions éloignées des conditions ambiantes (basse température, faible pression, ets.) pour éviter toute interférence avec l’environnement et ne sont souvent pas stables hors de leur lieu de fabrication. Il s’agit donc davantage d’une preuve de concept –fort élégante – que d’une solution technologique.
Les deux chemins vers le monde nano, top-down et bottom-up, sont parfois empruntés de concert pour aboutir à des structures originales. Par exemple, pour fabriquer des nano-voitures et autres machines moléculaires, la chimie organique est mise à profit pour préparer, à partir de petites molécules, les briques élémentaires (roues, axe, etc.). Puis les pièces sont assemblées en objets « supramoléculaires » (les pionniers de cette démarche ne sont autres que J.M-Lehn et J.P. Sauvage [5], tous deux prix Nobel de Chimie). Ces assemblages sont ensuite étudiés grâce aux outils d’imagerie de la voie top-down, par exemple la microscopie à force atomique2. Ceci peut donner lieu à des événements sportifs insolites, tels que des courses de nano-voitures, pour le plus grand bonheur de tous !3
Nanoparticules et Nanomatériaux du quotidien
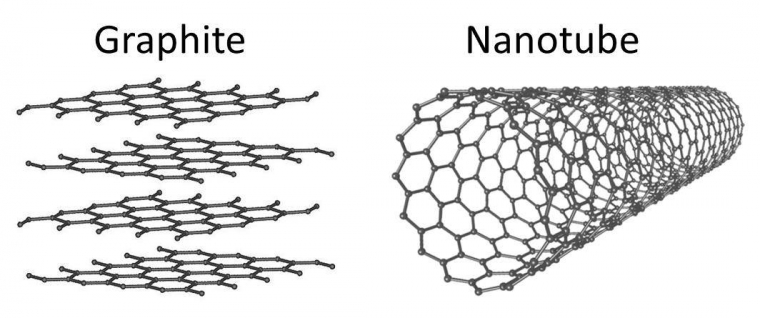
Les nanoparticules et nanomatériaux que l’on retrouve aujourd’hui sur le marché et dans l’industrie sont produits par des méthodes à grande échelle, directement apparentées aux procédés de fabrication de matériaux macroscopiques : matériaux à haute qualité mécanique, cosmétiques, verres intelligents, électrodes de batteries au lithium, etc. En termes de tonnage, il s’agit principalement des produits suivants (des exemples de domaines d’application sont donnés entre parenthèses) : nanoparticules de silice (additif alimentaire, renforcement de pneumatiques), de dioxyde de titane (cosmétique), d’alumine (additif alimentaire, adjuvant dans le domaine médical), d’oxyde de zinc (cosmétique) et de cerium (peinture), nanotubes de carbone (renforcement mécanique pour article de sport), fullerènes et noir de charbon (encres, électrodes de batteries au lithium), nanoparticules d’argent (anti-bactérien, verres à faible déperdition énergétique) et de fer (décontamination des sols), dendrimère4 (thérapeutique) et nano-argiles (absorbants). Pour tous ces produits, la matière première employée est commune, qu’il s’agisse d’un matériau minéral (ex. la silice) ou d’une molécule organique. C’est la mise en forme à l’échelle nanométrique qui est la clé de la nouvelle application. Par exemple, les structures en fibre des nanotubes de carbone sont à l’origine de nouvelles propriétés mécaniques, qui n’existent pas dans le graphite5 (Figure 2). De même, l’usage du dioxyde de titane comme absorbant du rayonnement ultraviolet dans les crèmes solaires requiert des particules submicroniques pour préserver la texture et l’aspect de la crème.
Illustration adaptée de Wikipédia.
Ainsi, le caractère nanoscopique ne permet pas de cerner, à lui seul, le potentiel des nanotechnologies ni les nouveaux risques associés aux nanomatériaux actuellement mis sur le marché. Il faut retenir à la fois l’idée de petite taille et celle de la présence d’une nouvelle propriété comme conséquence de cette taille réduite. C’est d’ailleurs ainsi que procèdent la plupart des définitions opérationnelles et institutionnelles.
Les nanoparticules : de curieux objets
La curiosité scientifique suscitée par les nanomatériaux provient autant de leurs nouvelles propriétés intrinsèques que de leur palette d’applications. Dans le cas des semi-conducteurs, on assiste à l’apparition d’un effet quantique à l’échelle nanométrique : alors qu’une diode électroluminescente macroscopique a une couleur fixée, des nanoparticules du même matériau auront une couleur dépendant directement de leur taille. Il en va de même pour d’autres propriétés fondamentales, comme la température de fusion : une nanoparticule d’or de 3 nm de diamètre devient liquide à une température deux fois plus basse que l’or massif.
Coloration de l’or nanométrique
Exposée au British Museum, cette coupe contient des nanoparticules d’or et d’argent. Si elle est éclairée par ses côtés (éclairage habituel), elle apparaît verte. Si elle est éclairée par l’intérieur, autrement dit en « transmission » (l’objet est alors entre la lampe et l’œil), elle apparaît rouge.
Des phénomènes physiques inédits apparaissent aussi à l’échelle nanométrique. Toujours dans le cas de l’or, une coloration rouge rubis apparait pour des particules d’une dizaine de nanomètres de diamètre. Cet effet est dû au comportement particulier du nuage électronique qui entoure la nanoparticule. Celui-ci entre en résonance avec certaines fréquences lumineuses et les absorbe préférentiellement. L’artisanat verrier utilisait d’ailleurs l’or dans la coloration rouge des verres et vitraux, appelée pourpre de Cassius, bien avant que l’on ne comprenne que le procédé de fabrication générait des nanoparticules. Un célèbre objet, la coupe de Lycurgus (Figure 3), met en scène cette couleur rouge profond pour illustrer une scène de la mythologie grecque dans laquelle le roi Lycurgus attaque Dionysos, dieu de la vigne et des excès.
Cette coloration spectaculaire, visible à l’œil nu, permit à Michael Faraday, dès le milieu du XIXe siècle, de réaliser que la matière avait de nouvelles propriétés pourvu qu’on en fasse des particules « extrêmement petites » [6]. Ce résultat témoigne autant de l’intuition expérimentale remarquable de ce chercheur touche-à-tout que de la fascination créée par l’or pourpre. Faraday avait développé plusieurs procédés de fabrication de nanoparticules d’or, en utilisant une décharge électrique dans un fil d’or, ou encore par voie chimique en solution. Il reportait dès 1857 que leur couleur dépendait de leur taille [7]. Ceci est probablement le premier travail expérimental systématique sur les nanoparticules. Il faut pourtant réaliser qu’à cette époque, les notions d’atomes et de molécules n’étaient pas encore fermement établies !
Sculpter la matière à l’échelle nanométrique
Depuis ces découvertes pionnières sur les nanoparticules d’or, les scientifiques ont beaucoup progressé dans la fabrication de nano-objets contrôlés à l’atome près. La chimie permet par exemple de fabriquer des nano-émetteurs appelés « boîtes quantiques », de couleur bien plus intense que les colorants traditionnels, très pure et très bien ajustée par le biais de leur diamètre (entre 2 et 10 nm), donc leur nombre d’atomes (Figure 4). Cela veut dire que non seulement le chimiste peut ajuster la longueur d’onde à loisir (alors que pour les colorants, il faudrait reconstruire une molécule différente à chaque fois), mais qu’en plus celles-ci sont émises dans un petit intervalle (là où un colorant traditionnel émet sur une gamme large). Ceux-ci sont utilisés comme marqueurs dans la recherche biomédicale, mais font aussi leur apparition sur le marché pour les technologies d’écran plat.
Nanoparticules de sélénure de cadmium dont l’absorption et l’émission varient en fonction du diamètre
Sur les nano-objets, la plupart des atomes sont exposés à la surface, car chaque atome mesure déjà un dixième de nm. Cette caractéristique de l’échelle nanométrique a des conséquences drastiques sur les propriétés des nanoparticules en général, comme illustré ci-dessous.
Nanoparticules et surface géométrique
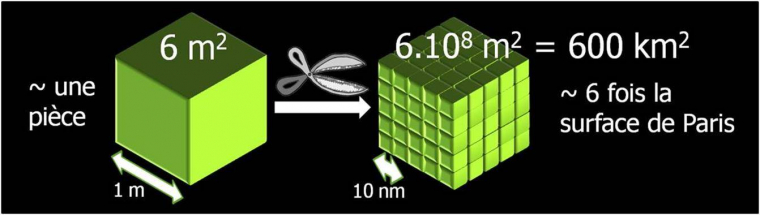
Puisque le nombre d’atomes constituant une nanoparticule est réduit (de quelques dizaines à quelques milliers), la proportion d’atomes exposés à sa surface est relativement grande par rapport à celle d’un matériau macroscopique. Par conséquent, un gramme de nanoparticules développe une surface incomparablement plus grande qu’un gramme de particules courantes, tels que des grains de sable. À titre d’exemple, prenons un cube d’un mètre de côté. Ce cube a une surface de 6m2, c’est-à-dire la surface d’une pièce. Le même volume constitué de nanocubes de 10 nm d’arête développe une surface de 600 km2, c’est-à-dire environ six fois la surface de Paris (Figure 5) ! Tout phénomène lié à la surface d’un matériau est donc exacerbé dans le cas de nanoparticules.
Mais deux conséquences supplémentaires, moins intuitives, entrent en jeu. D’une part, la surface est associée à un surcoût énergétique pour l’ensemble de la particule : on parle d’énergie de surface. De façon simple, on peut voir cette énergie supplémentaire comme l’énergie qu’il a fallu fournir pour découper le cube unique en des millions de petits cubes. Cet excès d’énergie implique que les nanoparticules sont plus « réactives » que des macroparticules, ou plus instables. D’autre part, les atomes à la surface d’une nanoparticule (ceux qui forment la dernière couche) n’ont pas le même environnement, et donc pas les mêmes propriétés, que les atomes du cœur de la nanoparticule : ils sont exposés au milieu extérieur et susceptibles de créer de nouvelles liaisons chimiques. Les propriétés des nanoparticules sont donc autant régies par les propriétés de leurs frontières que par leur constitution intrinsèque. Cela les rend très sensibles à l’environnement.
Chimie de surface sur des nanoparticules
Pour garder le cas de l’or, un exemple frappant est la capacité des nanoparticules d’or à provoquer des réactions chimiques entre les molécules d’un mélange gazeux auquel elles sont exposées. L’or massif, lui, est un métal extrêmement inerte ; c’est pourquoi il est utilisé pour les ouvrages de précision, pour les étalons ou pour recouvrir d’autres métaux plus sensibles à l’oxydation ou à la corrosion. Au contraire, les nanoparticules d’or sont très réactives. Elles « catalysent » la réaction d’oxydation du monoxyde de carbone en dioxyde de carbone à basse température (- 70°C), réaction d’équation CO + ½ O2 à CO2.Cela signifie qu’elles facilitent et accélèrent cette réaction qui nécessiterait sinon un apport d’énergie important (chauffage, etc.) pour avoir lieu.
Ce résultat remarquable datant des années 1980 est à l’origine d’un nouvel âge d’or (c’est le cas de le dire…) pour la catalyse [8-9]. Il constitue un exemple moins connu du rôle des nanoparticules dans le développement de technologies propres et peu consommatrices d’énergie. De la même façon, des nanoparticules de platine sont incorporées dans les pots catalytiques des voitures pour dépolluer les rejets gazeux des moteurs à combustion en accélérant la destruction des composés chimiques les plus nocifs (monoxydes d’azote et de carbone).
La catalyse : un domaine au cœur des nanosciences
De fait, le grand public ignore souvent le rôle que jouent les nanoparticules dans le domaine de la catalyse, probablement car ce domaine lui-même, pourtant primordial en termes d’impact économique et environnemental, est méconnu. Les phénomènes catalytiques sont en effet ubiquitaires. Le système enzymatique des organismes vivants est composé de catalyseurs moléculaires à l’œuvre à chaque instant pour effectuer à température ambiante des réactions chimiques, qui seraient extrêmement lentes sans catalyseur, à température ambiante. Par exemple, la photosynthèse des plantes vertes, c’est-à-dire la transformation du dioxyde de carbone en matière végétale, nécessite de casser des liaisons entre atome de carbone et atome d’oxygène et d’en former de nouvelles entre atomes de carbone, pour passer du dioxyde de carbone gazeux à des molécules organiques. L’équation simplifiée de la transformation de CO2 en glucose par la photosynthèse s’écrit : 6 CO2 + 6 H2O à C6H12O6 + 6 O2.
De même, la respiration des mammifères, c’est-à-dire la consommation de dioxygène pour produire de l’énergie, met en jeu des séquences de réactions catalytiques parfaitement ajustées dans le temps et dans l’espace grâce à des millénaires d’évolution biologique. De son côté, l’industrie utilise depuis sa fondation des catalyseurs artificiels, inspirés par les systèmes biologiques ou non, pour fabriquer les produits de l’agriculture (engrais azotés), de la grande consommation (plastiques, polymères) ou des transports (carburants), ou encore pour le recyclage et la dépollution.
On estime que 90 % des produits manufacturés dans le monde ont subi au moins une étape catalytique au cours de leur fabrication. Pour utiliser au mieux l’énergie et les matières premières que la planète nous offre, les industriels et les scientifiques cherchent à améliorer les catalyseurs existants, pour les rendre plus performants, moins coûteux et moins toxiques. Les nanoparticules et nanomatériaux sont des catalyseurs de choix car ils offrent une large palette de compositions et de propriétés, que l’on peut ajuster à loisir à la réaction recherchée. Les réactions chimiques se déroulent à la surface des nano-catalyseurs : leur grand état de division garantit une utilisation maximale du matériau. De plus la taille des nanoparticules influence leur façon de catalyser les réactions chimiques. Ceci permet de contrôler plus finement les réactions, et notamment, de favoriser la formation de certains produits par rapport à d’autres en fonction des besoins.
Depuis plus d’un siècle, de nombreux procédés industriels utilisent des nanoparticules. Parmi les plus essentiels, deux d’entre eux sont décrits ci-dessous : ils sont encore au cœur d’une recherche très active pour s’adapter aux contraintes toujours plus fortes sur la consommation énergétique et les matières premières.
Synthétiser des carburants
Le procédé Fischer-Tropsch, développé initialement dans les années 1920, permet de fabriquer à l’échelle industrielle des carburants à partir de sources de carbone abondantes telles que le charbon, la biomasse, etc. Ce procédé met en jeu des réactions d’équations : (2n+1) H2 + n CO → CnH(2n+2) + n H2O. Plusieurs valeurs de la grandeur n sont obtenues dans le procédé : de n = 1 (méthane) jusqu’à une dizaine. Il faut ensuite séparer les différents produits.
Son importance et son poids dans l’économie ne sont pas négligeables : ce procédé a garanti l’approvisionnement en hydrocarbures de l’Allemagne durant la Seconde Guerre, et par la suite de l’Afrique du Sud dans les années 1950. Il consiste à réassembler de façon contrôlée les atomes de carbone, d’oxygène et d’hydrogène contenu dans le mélange intermédiaire de gaz appelé « gaz de synthèse », obtenu par combustion incomplète de la matière première. Le rôle du catalyseur nanoparticulaire est de casser les liaisons chimiques du monoxyde de carbone et du dihydrogène et de former de nouvelles liaisons entre carbones, hydrogènes et oxygènes, afin de créer des hydrocarbures. Ces étapes sont très coûteuses en énergie. Le catalyseur, qu’il s’agisse de nanoparticules de cobalt, de nanoparticules de fer comme sur la Figure 1, ou autre, permet non seulement d’abaisser les températures et pressions requises, mais aussi de contrôler plus précisément la nature des molécules formées (en particulier, leur masse moléculaire et leur degré de saturation).
Aujourd’hui, en raison de la raréfaction du pétrole naturel, ce procédé redevient pertinent. Des efforts conséquents sont faits en recherche et développement pour optimiser les catalyseurs existants et en trouver de nouveaux. Par exemple, on sait désormais que la taille des nanoparticules joue un rôle critique dans leur aptitude à réagir avec le monoxyde de carbone, au tout début du cycle réactionnel. Pour le scientifique, le jeu consiste à fabriquer des nanoparticules de taille bien calibrées et à les tester les unes après les autres pour mieux comprendre le lien entre structure et réactivité des nanoparticules.
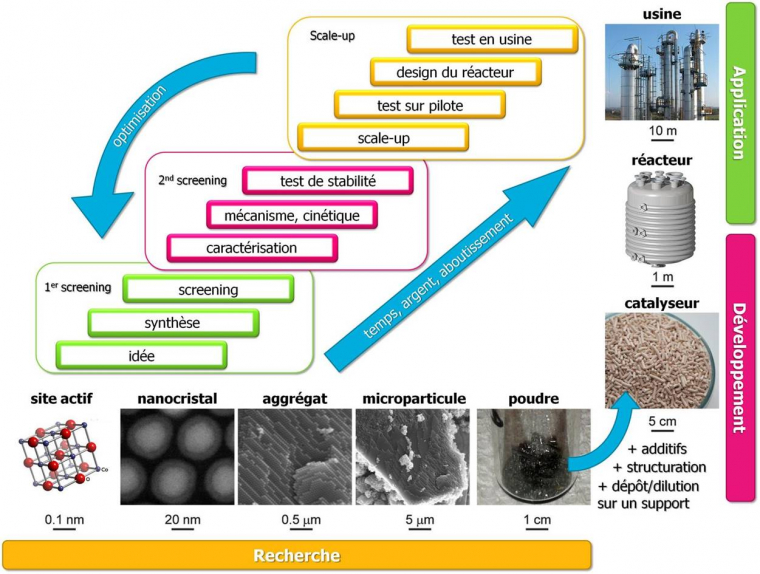
Mais pour passer à l’échelle industrielle, plusieurs étapes sont requises comme illustré sur la Figure 6. Elles mettent en jeu de multiples échelles et diverses spécialités techniques et scientifiques. La conception initiale du nanomatériau en termes de composition et de forme, puis sa structuration à échelle croissante, sont au cœur des avancées scientifiques et techniques. En ce sens, les « Nanosciences » sont un domaine cohérent à la croisée de plusieurs disciplines.
Le nanomatériau et les autres paramètres du procédé industriel font l’objet d’optimisation à plusieurs échelles. Illustration adaptée de [13].
L’azote pour nourrir la planète
Un autre exemple montrant le poids et le potentiel de la catalyse dans les questions énergétiques et environnementales est le procédé Haber-Bosch, datant de 1909. Ici, il s’agit d’utiliser le diazote, le gaz le plus abondant de l’atmosphère, et de le convertir en ammoniac (NH3) qui est la source pour fabriquer les engrais azotés. La réaction mise en jeu a pour équation N2 + 3 H2 à 2 NH3 ; elle requiert donc de casser la triple liaison azote-azote de N2, une étape très difficile, puis de faire réagir les atomes d’azote avec des atomes d’hydrogène (fournis par du dihydrogène gazeux). Ce procédé est très largement utilisé à l’échelle mondiale, car il garantit le rendement des récoltes via l’utilisation d’engrais synthétiques. Les catalyseurs modernes sont des nanoparticules de fer ou de ruthénium, déposés sur un support adéquat (silice, alumine, etc.) et améliorés par des additifs tels que le potassium : ces nanomatériaux présentent ici aussi une structure bien particulière, optimisée à toutes les étapes de la conception.
Malgré tout, les températures et pressions de fonctionnement sont encore élevées pour ce procédé (autour de 400°C et 200 bar). A titre de comparaison, les enzymes nitrogénases des plantes vertes réalisent la même transformation à 25°C et sous pression atmosphérique, mais avec un rendement bien moindre malheureusement… Le volume d’engrais azotés nécessaire chaque année sur l’ensemble de la planète est tel que ce seul procédé industriel consomme environ 1 % de l’énergie mondiale produite ! Il est trivial de dire qu’optimiser son rendement, même de quelques dixièmes de pourcent, contribuerait à réduire l’empreinteénergétique de notre civilisation. C’est pourquoi la recherche et le développement, du plus fondamental au plus appliqué, sont toujours extrêmement actifs en nanocatalyse.
Les nanomatériaux ne s’arrêtent pas là !
Ces deux exemples tirés du domaine de la catalyse illustrent le rôle primordial joué par les nanomatériaux, avant même l’apparition du mot nanosciences. Bien d’autres champs s’appuient aujourd’hui sur ces composés complexes et originaux pour progresser : le photovoltaïque, la vectorisation thérapeutique, le stockage de l’énergie et les batteries au lithium, etc. Leurs horizons dépassent le cadre parfois minimaliste du débat actuel qui entoure les « nanos ». De par la diversité de leur nature et de leurs applications, ces nouveaux matériaux soulèvent de nombreuses questions éthiques et toxicologiques de prime importance, que nous n’avons pas discutées ici. Leur potentiel outrepasse les applications telles que les crèmes solaires (nanoparticules d’oxyde de titane) ou les chaussettes antibactériennes (nanoparticules d’argent), qui sont bien plus souvent évoquées dans la presse « grand public ». La partie immergée de l’iceberg (la catalyse, les énergies propres, mais aussi la compréhension aboutie des propriétés de la matière…) nous semble plus que jamais pertinente dans une réflexion globale sur les « nanos ».
Bibliographie et références
Bibliographie
- Les nanotechnologies doivent-elles nous faire peur ? Louis Laurent, Jean-Claude Petit. Ed : LE POMMIER, Collection : Les Petites Pommes du Savoir, 2005.
- Nanosciences : La révolution invisible. C. Joachim, L. Plévert, éd. Seuil, 2008.
- Fascinantes nanotechnologies : Au-delà des grandes peurs, des grands doutes et des grands espoirs. Julie Dubois et François Rousseau, Presse des mines, 2009.
- Développons les nanomatériaux ! Fabrication, opportunités et gestion du risque. Sophie Carenco, Editions Rue d’Ulm, Collection Sciences durables, 2012.
Références
[1] INRS (institut national de recherche et de sécurité) : Dossier « Les nanomatériaux, définitions, risques toxicologiques, caractérisation de l’exposition professionnelle et mesures de prévention », M. Ricaud, O. Witschger, ED 6050, Juin 2008.
[2] https://fr.wikipedia.org/wiki/Lithographie_%C3%A0_faisceau_d%27%C3%A9lectrons.
[3] « Nanosciences : La révolution invisible », C. Joachim, L. Plévert, éd. Seuil, 2008, ISBN-13: 978-2020867030.
[4] http://www.research.ibm.com/articles/madewithatoms.shtml; http://www.youtube.com/watch?v=oSCX78-8-q0&feature=player_embedded.
[5] http://nanocar-race.cnrs.fr.
[6] http://link.springer.com/article/10.1007%2FBF03215598
[7] Michael Faraday, “Experimental relations of gold (and other metals) to light”, Phil. Trans., 1857, 145-181.
[8] Haruta, M., Kobayashi, T., Sano, H., Yamada, N., "Novel Gold Catalysts for the Oxidation of Carbon Monoxide at a Temperature far Below 0 °C", Chemistry Letters, 1987, 16, 405-40.
[9] Mitchell, S., Michels, N.-L., Pérez-Ramírez, J., “From powder to technical body: the undervalued science of catalyst scale up”, Chemical Society Review 2013, 42, 6094-6112.